EMA versäumt es, COVID 19-Impfstoffe vom Markt zu nehmen, obwohl das Nutzen-Risiko-Verhältnis gleich null ist
EU-Sicherheitsbericht zum mRNA-Impfstoff von Pfizer-BioNTech enthüllt vernichtende Daten
Es ist höchste Zeit, die EMA und die EU-Kommission sowie ihre mitschuldigen Partner – angefangen bei der WHO, der FDA und dem CDC – für ihre Pflichtverletzung zur Rechenschaft zu ziehen, weil sie die eklatanten Sicherheitssignale ignoriert und an der offensichtlich falschen Aussage festhalten, dass das Nutzen-Risiko-Profil des Impfstoffs COVID-19 von Pfizer-BioNTech weiterhin nützlich“ sei . Dieser seit langem vorliegende Sicherheitsbericht, der im August 2021 veröffentlicht wurde, dient als solider Beweis dafür, dass die Verantwortlichen Behörden, die die COVID Impfstoffe analysieren und für den Markt freigeben, sich der verheerenden Auswirkungen durchaus bewusst waren. Sie haben nicht nur ihrer Sorgfaltspflicht zur ordnungsgemäßen Bewertung von mRNA-„Impfungen“ vor der Verabreichung am Menschen versäumt, sondern ignorieren weiterhin die vorliegenden Sicherheitsindikatoren, was zu unermesslichem Schäden und Verletzungen führt.
Ihre wiederholte Weigerung, ihren gesetzlichen Auftrag zu erfüllen, erfordert eine Untersuchung möglicher zivil- und strafrechtlicher Verstöße, sowie ein Verfahren, um alle Beteiligten in die Verantwortung zu nehmen.
Orsolya Gyorffy, CHD Europa
Ursprünglich veröffentlicht von CHD Europe am 19. Februar 2023
Tippfehler und Schwangerschaftsausgänge geändert am 22. Februar 2023

EU-Sicherheitsbericht über den mRNA-Impfstoff von Pfizer-BioNTech enthüllt belastende Daten
Von Sonia Elijah
Der erste 286-seitige EU-Bericht über die regelmäßige Aktualisierung der Sicherheit(PSUR #1), der den sechsmonatigem Zeitraum vom 19. Dezember 2020 bis zum 18. Juni 2021 abdeckt, enthüllt vernichtende Sicherheitssignale für den Pfizer-BioNTech Covid-19-Impfstoff (COMIRNATY). Der Bericht wurde über eine FOIA-Anfrage eines anonymen Lesers veröffentlicht und dem österreichischen Wissenschafts- und Politikblog TKP zur Verfügung gestellt.
Nach der Definition der Europäischen Arzneimittelagentur sind PSURs Pharmakovigilanz Dokumente, die eine Bewertung des Nutzen-Risiko-Verhältnisses eines Arzneimittels in bestimmten zeitlichen Abständen, nach dessen Zulassung liefern sollen. Ziel des PSUR ist es, eine umfassende und kritische Analyse des Nutzen-Risiko-Verhältnisses des Arzneimittels vorzulegen, wobei neue oder sich abzeichnende Sicherheitsinformationen im Zusammenhang mit den kumulativen Informationen über Risiken und Nutzen berücksichtigt werden
Der Zulassungsinhaber (MAH), in diesem Fall BioNTech SE, ist gesetzlich verpflichtet, der EMA einen PSUR zusammen mit einer Antragsgebühr vorzulegen. Die EMA bewertet dann die im Bericht enthaltenen Informationen, um festzustellen, ob neue Risiken identifiziert wurden oder ob sich das Nutzen-Risiko-Verhältnis geändert hat.
Ich habe mich ausgiebig mit den umfangreichen Dokumenten von Pfizer-BioNTech im Zusammenhang mit Impfstoffen befasst, und dieser Bericht war einer der aufsehenerregendsten, nicht nur in Bezug auf die belastenden Daten, sondern auch auf die Schlussfolgerung, dass dasNutzen-Risiko-Profil von BNT162b2 weiterhin von Nutzen ist„
Die belastenden Daten
Im Folgenden finden Sie einen Überblick über die Gesamtzahl der Fälle (Daten nach dem Inverkehrbringen und aus klinischen Studien) im sechsmonatigen Berichtszeitraum:

Die nachstehende Tabelle (aus dem Dokument entnommen) zeigt die Anzahl der Fälle, aufgeschlüsselt nach Geschlecht, Alter, Land, Schweregrad des Falls, Ergebnis und Vorhandensein von Komorbiditäten.
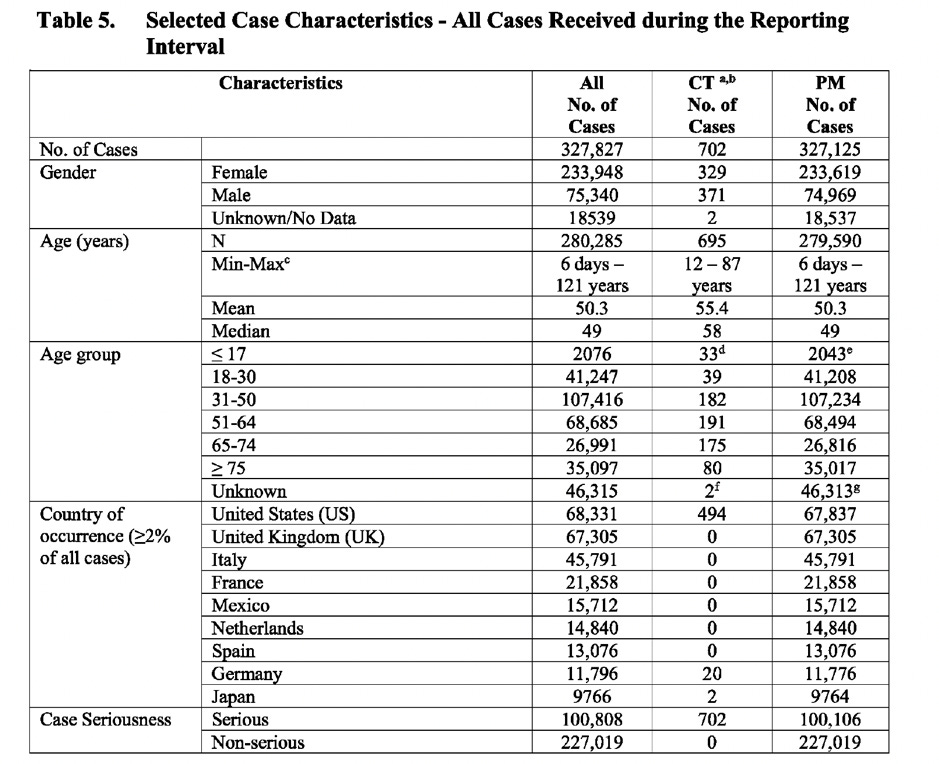
Tabelle 5. Regelmäßiger aktualisierter EU-Sicherheitsbericht für den 6-Monats-Zeitraum vom 19. Dezember 2020 bis zum 18. Juni 2021

CT: Daten aus der klinischen Prüfung PM: Post-Marketing-Daten
Bemerkenswert ist, dass ich bei der Analyse des von Pfizer für die FDA erstellten Dokuments mit dem Titel „Cumulative Analysis of Post-Authorization Adverse Event Reports of PF-07302048 (BNT162B2) received by 28 February 2021″ (Kumulative Analyse der Berichte über unerwünschte Ereignisse nach der Zulassung von PF-07302048 (BNT162B2), die bis zum 28. Februar 2021 eingegangensind) ähnliche Feststellungen in Bezug auf geschlechtsspezifische Sicherheitsrisiken für Frauen, Personen (Fälle), die im Durchschnitt an drei bis vier unerwünschten Ereignissen leiden, eine hohe Anzahl von Berichten mit entweder unbekanntem und/oder ungeklärtem Ausgang, eine hohe Anzahl von Fällen mit unbekanntem Geschlecht und die ungewöhnliche Gruppierung von genesenden/ in der Genesung befindlichen Fällen gefunden habe.
Ein auffälliger Unterschied zwischen den beiden Berichten ist jedoch die explosionsartige Zunahme der Anzahl von Fällen und Ereignissen, die im PSUR der EU aufgezeichnet wurden, und zwar um das Siebenfache im Vergleich zur Vorlage von Pfizer bei der FDA, die die Hälfte des Zeitraums abdeckt.
In dem Dokument heißt es, dass während des Berichtszeitraums schätzungsweise 635.763.682 Dosen weltweit verabreicht wurden, und es wird hinzugefügt: „Es ist nicht möglich, die Anzahl der Personen, die BNT162b2 während des Berichtszeitraums erhalten haben, mit Sicherheit zu bestimmen.“ Daher ist es nicht möglich, genaue Inzidenzraten zu extrapolieren.
Ein wichtiger Punkt, der bei der Bewertung der Daten berücksichtigt werden muss, ist jedoch das Ausmaß der Untererfassung von Fällen. Eine Harvard-Studie kam zu dem Schluss, dass nur 1-13 % der schwerwiegenden unerwünschten Ereignisse jemals gemeldet werden. Darüber hinaus lieferte eine systematische Übersichtsarbeit von Hazell et al. „Hinweise auf eine erhebliche und weit verbreitete Untererfassung von unerwünschten Nebenwirkungen in Spontanmeldesystemen, einschließlich schwerer oder schwerwiegender unerwünschter Nebenwirkungen“ Daher ist es besorgniserregend, dass, obwohl die Zahl der Fälle und Ereignisse im Berichtszeitraum hoch zu sein scheint, die tatsächlichen Zahlen weitaus höher gewesen sein könnten.
Die betroffenen jüngeren Altersgruppen ohne Komorbiditäten
Es ist bekannt, dass sich die meisten Menschen nach einer Covid-19-Infektion wieder vollständig erholen, insbesondere diejenigen, die keine Begleiterkrankungen haben und nicht älter sind. Der PSUR-Bericht enthüllt jedoch eine alarmierend andere Geschichte, wenn es um die Empfänger des Impfstoffs von Pfizer-BioNTech geht: erschütternde 23 % der Fälle von Personen, die nach der Impfung unter unerwünschten Ereignissen litten, erholten sich nicht (sie wurden nicht behandelt), und bei 21 % der Fälle war der Ausgang völlig unbekannt. Außerdem wurden die meisten Fälle in der Altersgruppe der 31- bis 50-Jährigen gemeldet, nicht in der älteren Bevölkerung. Bei der Analyse der Daten nach der Zulassung für tödliche Fälle, aufgeschlüsselt nach Vorhandensein/Nichtvorhandensein von Komorbiditäten, über alle Altersgruppen bis 64 Jahre hinweg, traten mehr tödliche Fälle bei Personen ohne Komorbiditäten auf. In der Altersgruppe bis 17 Jahre starben 22 Personen, die keine Komorbiditäten aufwiesen, gegenüber 1 Person mit einer Komorbidität. Erst in der Altersgruppe über 65 Jahre übersteigt die Zahl der Todesfälle mit Komorbiditäten die ohne Komorbiditäten. (Siehe Bildschirmfoto unten).
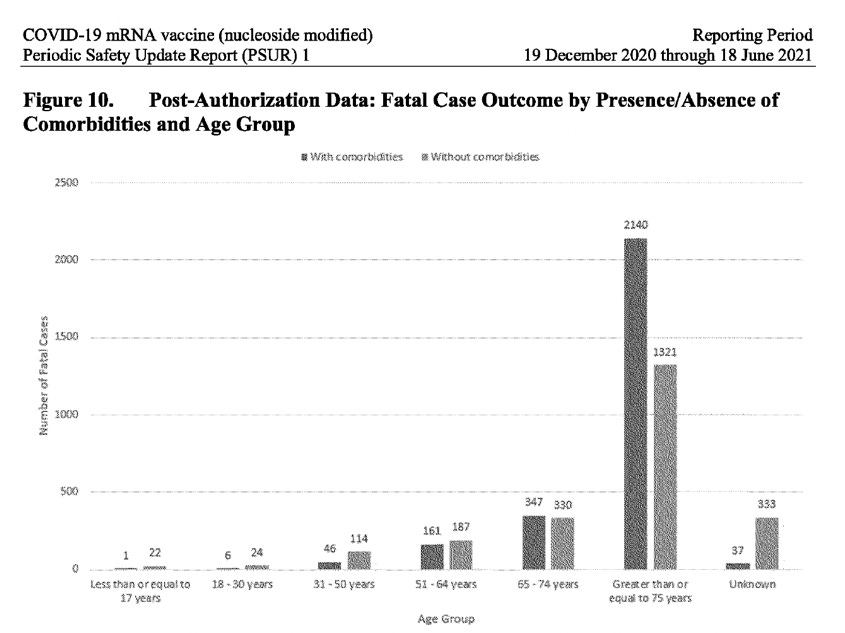
Es ist höchst ungewöhnlich, dass der PSUR dieses offensichtliche Sicherheitssignal, das jüngere Altersgruppen betrifft, nicht aufgreift, sondern stattdessen beschönigt, indem er sagt : „Insgesamt ist der Anteil der Fälle mit tödlichem Ausgang etwas höher, wenn Komorbiditäten gemeldet werden“
Der Fall von Maddie de Garay
Wenn man sich die Berichterstattung über die klinischen Studiendaten für die Altersgruppe der 12- bis 15-Jährigen in dem Dokument ansieht, fällt eine offensichtliche Auslassung auf, die man als Vertuschung des Falles von Maddie de Garay bezeichnen kann.
Anfang 2022 habe ich die Mutter von Maddie de Garay, Stephanie, interviewt. Maddie, damals 12 Jahre alt, nahm an der klinischen Studie von Pfizer/BioNTech für 12-15-Jährige teil. Kurz nach der Einnahme der zweiten Dosis erlitt Maddie lebensverändernde Verletzungen, so dass sie bewegungsunfähig und auf eine Ernährungssonde angewiesen war. Maddies Mutter erzählte mir, dass der leitende Prüfarzt der Pfizer-Studie für Jugendliche, Dr. Robert Frenck, die verheerenden Verletzungen ihrer Tochter als „Bauchschmerzen“ bezeichnete, obwohl ihm und den anderen Ärzten des Krankenhauses in Cincinnati alle ihre Symptome bekannt waren.
Beachten Sie, dass „Unterleibsschmerzen“ einer der PTs (bevorzugten Begriffe) in den relevanten Fällen ist, auf die im Screenshot unten für die Daten der klinischen Studie für 12-15-Jährige verwiesen wird.

Der PSUR wurde von der für die Pharmakovigilanz zuständigen EU-Beauftragten von Pfizer, Barbara de Bernardi, zwei Monate nach dem Stichtag 18. Juni 2021 abgezeichnet. Es ist ungewöhnlich, dass der CHMP der EMA den Impfstoff von Pfizer-BioNTech für Kinder im Alter von 12 bis 15 Jahren einen Monat vor der Fertigstellung des allerersten regelmäßigen Berichts über die aktualisierte Unbedenklichkeitsstudie der EU am 28. Mai empfahl und die EMA ihn nur wenige Tage später für diese Teilpopulation genehmigte. Warum wollte man nicht erst dieses wichtige Pharmakovigilanz-Dokument abwarten, das eine Bewertung des Nutzen-Risiko-Verhältnisses des Impfstoffs enthält, bevor man seine Entscheidung traf?
Die schlechten Chargen
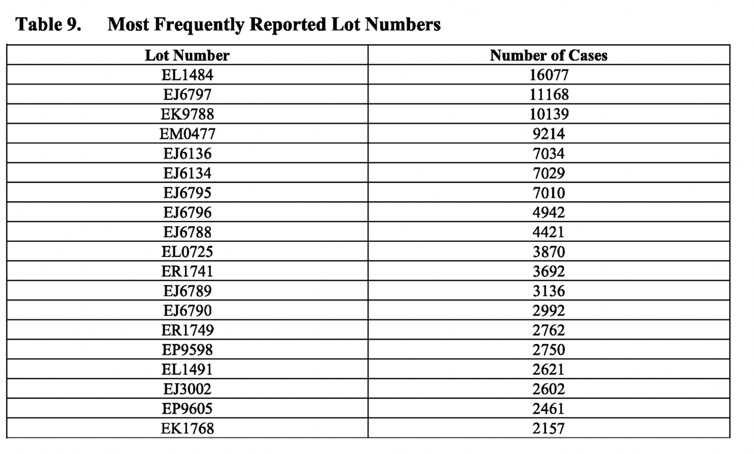
Die obige Tabelle zeigt die am häufigsten gemeldeten Chargennummern in Fallberichten. Man beachte die Häufigkeit von Fällen, die für bestimmte Chargennummern gemeldet wurden, wie z. B. die Chargennummer EL1484, die in 16 077 Fällen gemeldet wurde. Im PSUR heißt es jedoch weiter: „Insgesamt wurden bei den Untersuchungen dieser Chargennummern keine damit zusammenhängenden Qualitätsprobleme festgestellt, und alle potenziellen Signale, die auf einen möglichen Zusammenhang zwischen einem Sicherheitsproblem und einer bestimmten Chargennummer hindeuten und die nicht bereits im Rahmen anderer Signalaktivitäten bewertet wurden, würden gemäß den Standardverfahren bewertet und eskaliert“
Diese Aussage ist ausweichend – selbst der Begriff „insgesamt“ impliziert, dass es Probleme im Zusammenhang mit der Qualität gegeben haben könnte, die bei verschiedenen Chargen festgestellt wurden. Tatsächlich war dies aber bekannt. Ich habe ausführlich über die durchgesickerten EMA-E-Mails und andere Pfizer-BioNTech-bezogene Dokumente geschrieben, aus denen hervorging, dass die Aufsichtsbehörden bis zur Erteilung der Notfallzulassung Bedenken hinsichtlich der Schwankungen bei der Impfstoffqualität von Charge zu Charge hatten. In den kommerziellen Chargen des Impfstoffs wurde ein deutlich höherer Anteil an verkürzten (nicht intakten) mRNA-Spezies festgestellt als in den in den klinischen Studien verwendeten. Diese verkürzten Spezies wurden als „produktbezogene Verunreinigungen“ eingestuft
Bei der Suche in der Datenbank der Website HowBadIsMyBatch.com nach der oben genannten Chargennummer (EL1484) wurden die folgenden Informationen gefunden.
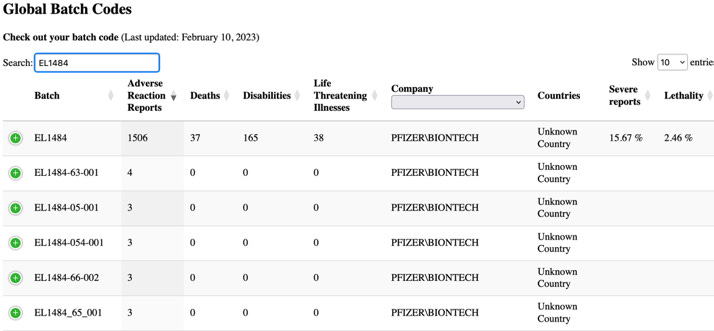
Das Ausmaß an schwerwiegenden Berichten und tödlichen Folgen, die von dieser Charge ausgehen, ist schockierend, doch scheint das EU-Dokument nichts Ungewöhnliches zu berichten.
Menstruationsbeschwerden
Interessant ist, dass es in dem Bericht heißt : „Im endgültigen AR [Bewertungsbericht] des5. SMSR [zusammenfassender monatlicher Sicherheitsbericht] vom 1. April 2021 bis 29. April 2021 wurde festgestellt, dass eine Reihe von Anfragen zu Menstruationsstörungen, insbesondere Menorrhagie [verlängerte Blutungen], eingegangen sind. Dieses Thema sollte im kommenden PSUR weiter untersucht werden, da es für junge Frauen von Bedeutung sein kann
Weiter heißt es : „Der MAH [BioNTech] wird gebeten, in diese PSUR-Überprüfung eine separate „Bewertung der Fälle nach dem Inverkehrbringen“ der Fälle aufzunehmen, in denen über Menstruationsstörungen berichtet wurde, die auch eine Unteranalyse der Fälle umfassen sollte, die in Fälle nach der Menopause und Fälle von Menstruationsstörungen unterteilt sind. Die Bewertung der Kausalität sollte für jeden Fall, zumindest für die schwerwiegenden Fälle, vorgelegt werden..
Diese Informationen wurden angeblich in Anhang 6B.6 „MENSTRUKTURSTÖRUNGEN“ bereitgestellt

Die FOIA-Veröffentlichung dieses PSUR enthielt jedoch keinen der wichtigen Anhangspunkte.
Die Schlussfolgerung der PSUR-Untersuchung zu Menstruationsstörungen ist bemerkenswert abweisend und wird von manchen sogar als beleidigend empfunden: „Diese stehen wahrscheinlich im Zusammenhang mit psychischen Belastungen und Stress im Zusammenhang mit der Pandemie, Gewichtszunahme, längeren Arbeitszeiten und Ernährungsumstellung…“
Ein Bericht, der im British Medical Journalkurz nach der Verabschiedung dieses PSUR veröffentlicht wurde, heißt es: „Veränderungen der Periode und unerwartete vaginale Blutungen sind nicht aufgeführt, aber Ärzte in der Primärversorgung und im Bereich der reproduktiven Gesundheit werden zunehmend von Personen angesprochen, die diese Ereignisse kurz nach der Impfung erlebt haben. Bis zum 2. September 2021 wurden dem MHRA-Überwachungssystem für unerwünschte Arzneimittelwirkungen (Yellow Card Surveillance Scheme) mehr als 30 000 solcher Ereignisse gemeldet, und zwar für alle derzeit angebotenen Covid-19-Impfstoffe
Darüber hinaus wurde im Juli 2022 eine systematische Überprüfung online verfügbar gemacht und in der wissenschaftlichen Zeitschrift ‚Vacunas‘ mit dem Titel: „Menstruationsanomalien nach COVID-19-Impfstoffen: A systematic review
Insgesamt wurden 78.138 geimpfte Frauen aus 14 Studien in die Überprüfung einbezogen. Dabei wurde festgestellt, dass bei einer signifikanten Anzahl von Frauen (52,05 %) nach der COVID-19-Impfung Menstruationsanomalien aufgetreten sind
Auswirkungen auf die Schwangerschaft
Einer der alarmierendsten Datensätze, auf die ich gestoßen bin, fällt in diese Kategorie. Ab Frühjahr 2021 begannen die Gesundheitsbehörden in den meisten Industrieländern, schwangere und stillende Frauen zu ermutigen, sich mit dem neuen mRNA-Impfstoff impfen zu lassen. Die vernichtenden Daten im PSUR, der im Sommer 2021 unterzeichnet wurde, hätten diese Behörden zu einer abrupten Kehrtwende veranlassen müssen, was jedoch nicht geschah.

Auf der Grundlage des oben genannten Ersuchens der WHO untersuchte der MAH (BioNTech) das Ergebnis der in den Daten der klinischen Studie beobachteten Schwangerschaftsfälle. Die nachstehende Tabelle 39 zeigt 26 Schwangerschaftsergebnisse von den 149 einzelnen Schwangerschaftsfällen, die während des Berichtszeitraums aufgezeichnet wurden. Von diesen 26 Ergebnissen führten 15 zu einem Spontanabort (Fehlgeburt) und 5 der Schwangerschaftsergebnisse führten zu Lebendgeburten mit angeborenen Anomalien.
Siehe die nachstehende Tabelle.

Als Reaktion auf diese alarmierenden Daten wurde in dem Bericht lediglich festgestellt: es lagen nur begrenzte Informationen über die geburtshilfliche Vorgeschichte der Mutter vor, was eine aussagekräftige Kausalitätsbewertung ausschloss
Todesfälle
Was die Datensätze zu Todesfällen (mit tödlichem Ausgang) anbelangt, so zeigt der folgende Screenshot die am häufigsten gemeldeten Todesursachen aus den Daten nach der Bewilligung.

Während des Berichtszeitraums war COVID-19 die häufigste Todesursache (neben dem „Tod“ selbst) – genau die Krankheit, gegen die der Impfstoff angeblich schützen sollte. Beachten Sie auch, dass der „plötzliche Tod“ als eine der häufigsten Ursachen angegeben wurde. Viele Berichte in den Mainstream-Medien (nach Einführung des COVID-19-Impfstoffs) berichteten über junge und gesunde Menschen, die plötzlich starben, was alarmierend ist.
Seltsamerweise wurden Autopsieberichte nur für 189 der 5042 Fälle aus den Daten nach der Zulassung vorgelegt. Die Ergebnisse sind im folgenden Screenshot zu sehen.

Eine Lungenembolie wird durch einen Thrombus verursacht, der sich in einer großen Vene, oft in den Beinen, bildet, sich ablöst und vom Blutstrom in die Lunge getragen wird, wo er dann eine der Arterien verstopft. Dies war die am häufigsten gemeldete Krankheit in den vorgelegten Autopsieergebnissen. Bemerkenswert ist, dass die US-amerikanische Gesundheitsbehörde FDA im Juli 2021 den Impfstoff von Pfizer-BioNTech mit vier neuen unerwünschten Ereignissen in Verbindung brachte, wobei sie jedoch hinzufügte, dass es keine Beweise für einen kausalen Zusammenhang gäbe. Dazu gehörten eine Lungenembolie, ein akuter Myokardinfarkt (Herzinfarkt), eine Immunthrombozytopenie (eine Bluterkrankung) und eine disseminierte intravasale Gerinnung (ein Zustand, bei dem sich Blutgerinnsel im ganzen Körper bilden).
In der Schlussfolgerung des PSUR zu den Todesfällen heißt es: „Die Überprüfung dieser Fälle hat keine neuen Sicherheitssignale ergeben… die Sicherheitsüberwachung wird fortgesetzt“
In Bezug auf die Immunthrombozytopenie heißt es in der Zusammenfassung des Berichts:

Es ist erstaunlich, wie der allererste EU-Pharmakovigilanzbericht für den Impfstoff COVID-19 von Pfizer-BioNTech, der mit solch belastenden Daten gespickt war, am Radar der Europäischen Arzneimittel-Agentur vorbeiging, ohne irgendwen in Alarmbereitschaft zu versetzen, und stattdessen die Schlussfolgerung zog, dass „das Nutzen-Risiko-Profil von BNT162b2 weiterhin von Nutzen ist“ Zu diesem Zeitpunkt gab es keine langfristigen Sicherheitsdaten, auf die sich die EMA stützen konnte, aber die kurzfristigen Daten (die seit Sommer 2021 bekannt sind) hätten die Alarmglocken läuten lassen müssen, aber das taten sie nicht, stattdessen wurde dieses experimentelle Produkt jüngeren Altersgruppen der Bevölkerung und schließlich Babys im Alter von nur 6 Monaten angeboten.
Angesichts der sprunghaft ansteigenden Sicherheitssignale, die in verschiedenen Überwachungsprogrammen für Impfstoffe nach dem Inverkehrbringen rund um den Globus beobachtet wurden, der alarmierenden Ergebnisse in den Dokumenten zu den klinischen Versuchen von Pfizer und BioNTech, der durchgesickerten EMA-Bewertungsberichte und internen E-Mails sowie der vernichtenden Daten, die im PSUR Nr. 1 gefunden wurden – all das hat als Katalysator gedient, um dringend alle anderen wichtigen Pharmakovigilanzberichte ans Licht zu bringen.
Ärzte und medizinische Experten in ganz Europa haben nun weitere Berichte mit einem ordnungsgemäßen Verfahren angefordert – weitere Analysen werden veröffentlicht, sobald wir Zugang dazu erhalten.
Um eine Korrektur vorzuschlagen, senden Sie eine E-Mail an: Karen@chdeurope.org







