Razkrito pismo vodje agencije EMA poslancem Evropskega parlamenta kaže na skrajno neuspešno delovanje agencije

Pred kratkim sem prejel osemstransko pismo (z datumom 20. aprila), ki ga je izvršni direktor Evropske agencije za zdravila EMA (in nekdanji lobist velike farmacije) Emer Cooke’ova poslala predsednici posebnega odbora COVID, evropski poslanki Kathleen Van Brempt. Prepričan sem, da bo nedvomno kmalu objavljeno na spletni strani agencije EMA v okviru njene “zavezanosti preglednosti”.
Pismo Emer Cooke-ove lahko naložite tukaj.
Njeno pismo je odgovor na nadaljnja vprašanja, ki so jih zastavili različni poslanci Evropskega parlamenta, kot so Robert Roos, Christine Anderson, Francesca Donato in Cristian Terhes v zvezi s cepivi COVID-19 mRNA, ki so bila izpostavljena na sejah posebnega odbora za pandemijo COVID-19.
Pred tem sem že pisal o pomembnih vprašanjih, ki jih je Roos zastavil Emer Cooke-ovi na seji Posebnega odbora za COVID-19 27. marca, in ovrgel številne neznanstvene neresnice, ki jih je navedla med svojimi umotvori in zmotami.
Nič drugače ni z osem strani dolgim pisnim odgovorom gospe Cooke.
Začne se s prikrivanjem zaskrbljujočih podatkov neklinične biodistribucijske študije, ki so januarja 2021 (približno na začetku uvajanja cepiva mRNA) objavila avstralska agencija Therapeutics Goods Administration (TGA). V njem je očitno zamolčano dejstvo, da so se lipidni nanodelci (dve od štirih lipidnih spojin sta povsem novi ter zelo strupeni in povzročajo vnetja) kopičili v jajčnikih podganjih samic.
V pismu je vsaj “priznala, da se lahko lipidni nanodelci precej nespecifično razporedijo v več organih, kot so jetra, vranica, srce, ledvice, pljuča in možgani, pri čemer se zdi, da se nanodelci najbolj zadržujejo v jetrih.“
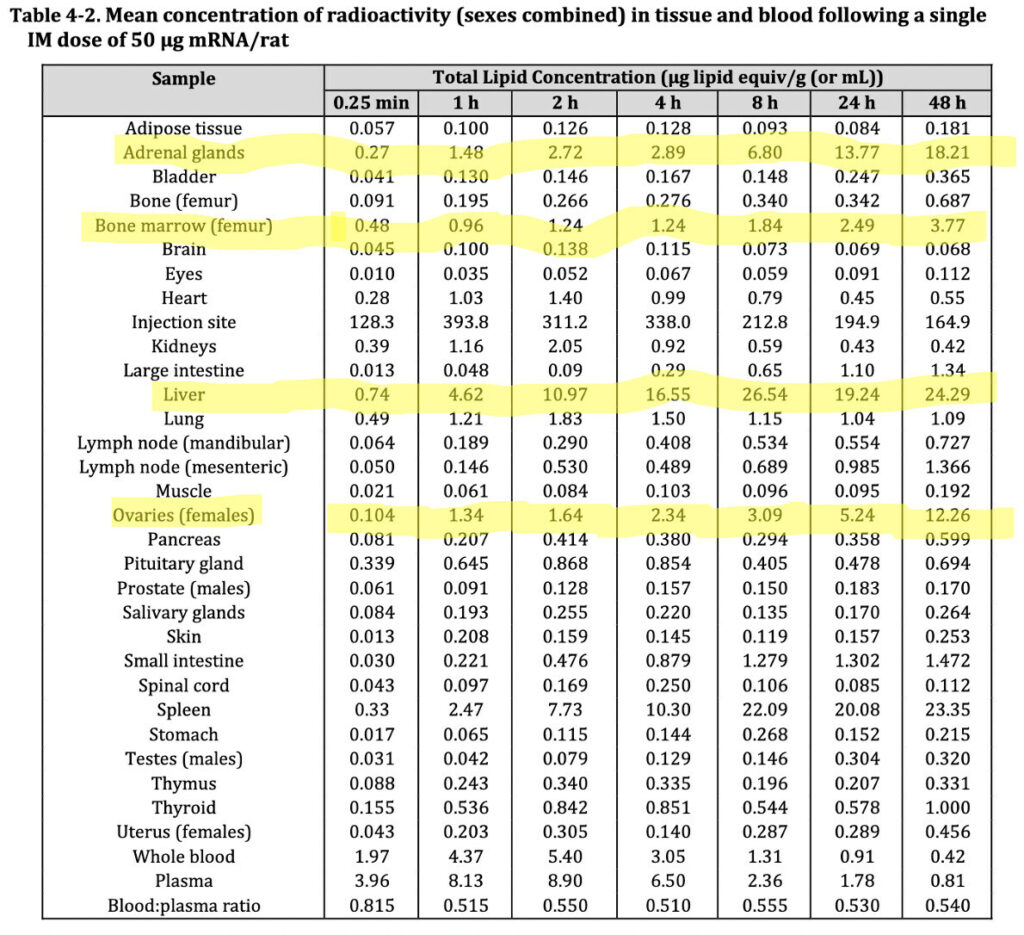
Njena namerna uporaba izraza “precej nespecifično” je očiten poskus zameglitve dejstva, da so se ti LNP (lipidni nanodelci) kopičili v skoraj vseh organskih tkivih, kot je razvidno iz zgornje preglednice, ki je povzeta iz poročila TGA o nekliničnem ocenjevanju – in v njenem pismu ni prikazano.
Omenja neklinične študije ponovnih odmerkov in biološke porazdelitve (farmakokinetične študije), “ki kažejo, da širša biološka porazdelitev ne predstavlja varnostnega problema.”
Vendar izpusti dejstvo, da rezultati študije biološke porazdelitve (farmakokinetične študije) niso bili potrjeni, niso bili izvedeni v skladu z DLP (dobra laboratorijska praksa) in niso preučevali porazdelitve dejanske modRNA, tiste v cepivu Pfizer-BioNTech COVID-19 (BNT162b2 ), ampak je bila namesto nje uporabljena nadomestna modRNA luciferaza. (Glej spodnjo sliko zaslona z razkritim poročilom poročevalca o oceni v okviru tekočega pregleda iz novembra 2020)

Biodistribucija nadomestnega reporterja luciferaze v obliki LNP: Za določitev biodistribucije formulirane modRNA vlagatelj ni preučeval distribucije modRNA, uporabljene v cepivu kandidata BNT162b2, temveč je v študiji brez DLP določil biodistribucijo nadomestne modRNA luciferaze, formulirane z LNP z enako sestavo lipidov, kot je uporabljena v cepivu BNT162b2. Ker je bilo v študiji testiranih več formulacij LNP, ni povsem jasno, katera od formulacij LNP se uporablja v klinični različici cepiva BNT162b2 (OC).
V študiji so bili uporabljeni trije samice miši BALB-c v skupini, izražanje beljakovine luciferaze pa je bilo določeno z odčitavanjem bioluminiscence in vivo z uporabo sistema za slikanje in vivo (IVIS) po injiciranju luciferaznega substrata luciferina. Odčitki so bili opravljeni 6 ur, 24 ur, 48 ur, 72 ur, 6d in 9d po injiciranju (predvidena klinična pot) v desno in levo zadnjo nogo s po 1 μg (skupaj 2 μg) luciferaze RNA, formulirane z LNP. Metoda biološke porazdelitve ni bila potrjena ali kvalificirana in ni bila vključena razprava o njeni občutljivosti. (ok).
Šokantno je, da niso bile opravljene nobene neklinične študije (na živalih) o biološki porazdelitvi dejanske modRNA, ki kodira cepilno beljakovino spike SARS-CoV-2, preden je bila vbrizgana ljudem! Vsi regulatorji so v veliki meri domnevali, da se bo modRNA, ki kodira beljakovino cepiva, porazdelila po telesu na popolnoma enak način kot luciferaza.
V svojem pismu z dne 20. aprila 2023 je zapisala, “razpoložljivi dokazi kažejo, da je količina mRNA, ki se porazdeli po telesnih organih, zelo majhna in se razgradi v 6-9 dneh po injiciranju.”
Naj ponovimo, da v dveh študijah biološke porazdelitve na živalih (mimogrede, v eni študiji, R-20-0072, so bile uporabljene le tri miši!) nikoli niso testirali dejanske modificirane mRNA, uporabljene v cepivu.
Spremenjena mRNA v cepivu Pfizer-BioNTech je sintetična. Vsak uridin je bil nadomeščen z N1-metilpseudourinom, da bi se izognili prirojenemu imunskemu odzivu telesa in spodbuja prevajanje beljakovin. Ker ni naraven, se ne razgradi hitro in iz tega dejstva izhajajo številne varnostne težave, na primer sprožitev avtoimunskih bolezni.
Evropska agencija za zdravila je imela to na svojem radarju od novembra 2020.

ModRNA vsebuje zamenjavo 1-metil-pseudouridina z uridinom. Ta zamenjava zmanjša prepoznavanje RNA cepiva s strani senzorjev prirojenega imunskega sistema, kot sta toll-like receptorja (TLR) 7 in 8, zaradi česar se zmanjša aktivacija prirojenega imunskega sistema in poveča prevajanje beljakovin. Pričakuje se, da bo cepljenje z modRNA povzročilo močna nevtralizirajoča protitelesa in hkratni odziv celic T, da se doseže zaščitna imunost. Kljub temu ni bila predložena nobena nadaljnja razprava o tveganju avtoimunskih odzivov, ki jih povzroča modRNA. Vlagatelj naj dodatno razpravlja o možnosti, da lahko cepivo mRNA sproži morebitne avtoimunske odzive, in o tem, kako namerava morebitno oceniti njihov pojav (MS-IT).
Obširno sem pisal tudi o razkritih elektronskih sporočilih agencije EMA in dokumentov družbe Pfizer(1. in 2. del ) iz novembra 2020, ki so zaskrbljujoče pokazali, da je stopnja celovitosti mRNA v komercialnih serijah cepiva padla na 55 % v primerjavi s kliničnimi serijami ~ 78 %. Raven RNK je merilo, kako nedotaknjen je zapis RNK – nižja kot je raven, večja je koncentracija skrajšanih ali fragmentiranih vrst RNK (ki niso nedotaknjene). Ključni regulatorji so se tega problema zavedali, vendar so ga vseeno odobrili, saj so sprejeli znižanje standarda celovitosti RNK na 50 %! Tako je bilo dovoljeno, da je do polovice molekul RNK v cepivu skrajšanih. Seveda v njenem pismu nič od tega ni bilo omenjeno.
To vodi do mojega poročanja o škandalu #Blotgate(1. in 2. del ), ki prikazuje dokaze, da je družba BioNTech ponaredila svoj test Western blot (tehnika, ki se uporablja za identifikacijo določenih beljakovin), s katerimi je EMA in drugim regulatorjem “dokazovala”, da je cepivo primerljivo med različnimi serijami in da se s cepilno mRNA izraža samo beljakovina spike.
Ocenjevalci agencije EMA so bili zaskrbljeni, da bi te skrajšane vrste mRNA lahko izražale tudi druge beljakovine, ne le predvidene beljakovine spike, zato so želeli, da se jih dodatno opredeli. Želeli so tudi, da bi družba BioNTech ocenila njihovo možnost, da “povzročijo avtoimunski proces”, glejte spodnji posnetek zaslona iz prečiščenega poročila CHMP iz avgusta 2021. Vidite lahko, da do izteka leta 2021 to še vedno ni bilo opravljeno in do danes ni bilo nobenega dokaza, da je bilo to sploh kdaj opravljeno.

potrebno je navesti prevladujoče vrste. Oceniti je treba vsako homologijo med prevedenimi beljakovinami (razen beljakovine spike) in človeškimi beljakovinami, ki lahko zaradi molekularnega posnemanja potencialno povzročijo avtoimunski proces. Rok za oddajo: julij 2023. Vmesno poročilo: Marec 2021 in mesečno.
V istem poročilu CHMP agencije EMA je bila družbi BioNTech naložena nova obveznost, ki jo je morala izpolniti – zahteva, da se enaka karakterizacija izvede za vsaj tri dodatne serije tozinamerana (spremenjena mRNA, zdravilna učinkovina). Kot lahko vidite, ta zahteva do julija 2021 ni bila izpolnjena.

Novo priporočilo (sklic: SO1a): Ni izpolnjeno 27. Uprava za varno hrano in veterinarstvo bi morala dopolniti postopek karakterizacije z uporabo sistema za prevajanje in vitro brez celic z dodatnimi serijami tozinameran (vsaj tremi), ki predstavljajo razpon od nizkih do visokih ravni celovitosti RNA ob sproščanju.
Poročilo o oceni skupine sprememb tipa II
EMA/CHMP/448917/2021 Stran 110/111
In glede na zadnjo posodobitev (2. februar 2023) Comirnaty: EPAR, ta obveznost še vedno ni izpolnjena.

V zvezi s SO1 je imetnik dovoljenja za promet zagotovil dodatne podatke o značilnostih, kot je bilo zahtevano.
a) Potencial skrajšanih transkriptov za proizvodnjo proteinov/peptidov je bil dodatno raziskan z uporabo brezceličnega in vitro ekspresijskega sistema. Poleg pasov ozadja, opaženih v negativnem kontrolnem vzorcu, ni bilo zaznati nobenih skrajšanih ali drugih vrst beljakovin. MAH bo dopolnil postopek karakterizacije z uporabo sistema za prevajanje in vitro brez celic z dodatnimi serijami tozinamerana.
Neverjetno je, da Cooke v svojem pismu (glej spodnjo sliko zaslona) navaja, da“podjetja, ki razvijajo in tržijo cepiva z mRNA, izvajajo načrtovane dodatne neklinične študije…. za nadaljnjo opredelitev in oceno biološke porazdelitve in razgradnje mRNA in beljakovine spike. Rezultati teh študij bodo predloženi v oceno agenciji EMA v letih 2023 in 2024.”

Za zaključek na temo biološke porazdelitve bi rad dodal, da podjetja, ki razvijajo in tržijo cepiva z mRNA, izvajajo načrtovane dodatne neklinične študije poleg tistih, ki so obravnavane v javnih poročilih o oceni EMA, da bi dodatno opredelila in ocenila biološko porazdelitev in razgradnjo mRNA in beljakovine spike. Rezultati teh študij bodo agenciji EMA predloženi v oceno leta 2023 in 2024.
Ne navaja, da je bil leto za izvedbo teh študij julij 2021, vendar jih “podjetja” niso nikoli izpolnila Iz njenega pisma je razvidno, da so bile te kritične študije prestavljene na leti 2023 in 2024!
To je dokaz, da agencija EMA ne namerava zahtevati posebnih obveznosti, ki jih je od konca leta 2020 naložila družbama BioNTech in Pfizer.
Omeniti velja, da je največja tovrstna študija iz Univerzitetne bolnišnice kralja Fahada v Khobarju v Savdski Arabiji povezala cepiva mRNA s sprožitvijo avtoimunskih bolezni, o čemer so poročali na TrialSite. V prej omenjenem poročilu agencije EMA je bila kot zaskrbljujoča navedena “molekularno posnemanje (mimikrija)”, ki je v študiji predstavljena kot mehanizem, povezan s tem, da cepiva mRNA povzroča avtoimunski proces.
Kevin McKernan je v intervjuju z vodilnim znanstvenikom na področju genomike in vodjo raziskav in razvoja pri projektu človeškega genoma izjavil:“Imamo izdelek mRNA, v katerem je vsak uridin zamenjan z N1 metilpseudourinom, ki ga telo še nikoli ni videlo. Izbrali so [BioNTech in Pfizer] stop kodone, ki so najbolj znani za ustvarjanje napak. Zavedala sta se težav, vendar je nista ustrezno odpravila. To pomeni, da so ribosomi, ko preberejo šablono, zelo zmedeni, saj je še nikoli prej niso videli.”
McKernan je skupaj z dr. Petrom McCulloughom in Anthonyjem Kyriakopoulosom napisal članek z naslovom “Razlike v mRNA, pridobljeni s cepivom in replikacijo SARS-CoV-2:(Differences in Vaccine and SARS-CoV-2 Replication Derived mRNA): (Pomen za celično biologijo in prihodnjo bolezen) Avtorji so ugotovili, da “sinonimne spremembe kodonov, vključene v cepivo mRNA, lahko spremenijo pričakovani zapis kodiranega proteina, saj lahko hitrost in učinkovitost prevajanja povzročita drugačno zlaganje proteina… Strategije optimizacije kodonov za razvoj cepiv mRNA lahko povzročijo imunske nepravilnosti, vplivajo na epi-transkripcijsko regulacijo in lahko vodijo v napredovanje bolezni
ŠtudijaRöltgenaindrugih, objavljena v reviji Cell, je razkrila, da modificirana mRNA v cepivih ter “antigen in mRNA cepilne špice več tednov obstanejo v človeških brezgavkah”

Cell – Immune imprinting, breadht of variant recognition and germinal centre responses in human SARS-CoV-2 infection and vaccination (Imunski vtis, širina prepoznavanja različic in odzivi zarodnega centra pri okužbi s SARS-CoV-2 in cepljenju). Korespondenca – publoations_scott boyd@stanford.edu. Odzivi človeških protiteles na SARS-Cov-2 se razlikujejo med cepljenjem in okužbo, pri čemer cepljenje mRNA povzroči produktivnejše odzive GC bezgavk, več vrst cepiv pa spodbudi protitelesa IgG, ki so sposobna prepoznati širši nabor virusnih različic.
‘ANTIGEN ZA CEPIVO SPIKE IN MRNA SE VEČ TEDNOV OHRANJATA V ČLOVEŠKIH BEZGAVKAH * … NE LE 9 DNI!
Povzetek:
- Cepljenje povzroči širšo vezavo IgG za različice RBD kot okužba s SARS-CoV-2
- Vtisi iz začetne izpostavljenosti antigenom spremenijo odzive IgG za virusne različice
- Histologija bezgavk cepljenih ljudi z mRNA, kaže obilnost GC
- Antigen spike v cepivih in mRNA se v GC limfnih vozlih ohranijo več tednov
Cooke je dolžna omeniti to študijo v reviji Cell, zahvaljujoč poslancu Evropskega parlamenta Robertu Roosu, ki se je nanjo skliceval v “naknadnem pismu”, naslovljenem nanjo. V njem pavšalno zapiše:“Lahko potrdimo, da so to študijo pregledali naši znanstveni strokovnjaki in da ne spreminja splošne ocene koristi in tveganja …”
Druga študija, ki so jo izvedli Castruita in drugi , je pokazala, da špice iz sekvenc mRNA cepiva SARS-CoV-2 krožijo v krvi do 28 dni po cepljenju s cepivom COVID-19.
Dejstvo, da Cooke še vedno vztraja pri napačni predstavi, da se mRNA razgradi hitro, v 6-9 dneh, glede na količino dokazov, ki jih imamo zdaj – jo obtožuje širjenja napačnih informacij.
Cooke si drzne še naprej pisati, da ” študije na živalih podajajo razumno zagotovilo, da pri cepljenju ljudi ni pričakovati varnostnih težav zaradi časovnega kopičenja lipidnih nanodelcev in mRNA v organih. “
Farmacevtko Marijo Gutschi, PharmD, sem vprašal o teh posebnih študijah na živalih. Gutschi, ki ima več kot 30 let izkušenj v bolnišnicah, lokalnih skupnostih in državnih upravah, je neodvisno analiziral težave s kakovostjo cepiva Pfizer/BioNTech, ki jih je ugotovila Evropska agencija za zdravila, in jih predstavila v informativnem videoposnetku.
Obvestila me je: “Podatki o varnosti, ki jih je izvedla družba Pfizer/BioNTech, so vključevali dve študiji toksičnosti s ponovnim odmerjanjem na podganah. Preučevali so različne prototipe mRNA, vključno s tistimi, ki kodirajo receptorsko vezavno domeno, samoamplificirajočo se RNK ter dve različici BNT162b2 (V8 in V9). Uporabljena je bila le celotna formulacija, zato ni toksikoloških podatkov o samih LNP [lipidnih nanodelcih] ali posebnih novih pomožnih snoveh. Agencija EMA je ugotovila, da so bili v študijah toksičnosti pri ponovnih odmerkih na podganah ugotovljeni funkcionalni učinki na jetra in/ali žolčnik; ti so vključevali povečane hepatocelularne in periportalne vakuolacije ter ravni jetrnih encimov. Histopatologija podgan, usmrčenih 17. dan, je pokazala vnetne znake na mestu injiciranja, perinevralnem tkivu sedečega živca in okoliških kosti. Opazen je bil tudi pomemben hematološki odziv, vključno z zelo močnim povečanjem števila nevtrofilcev, eozinofilcev in bazofilcev ter proteinov akutne faze in zmanjšanjem parametrov eritrocitov. Vranica je pokazala povečano krvotvorbo pri polovici živali na 17. dan. Edem in eritem na mestu injiciranja sta se z vsakim injiciranjem povečala, bezgavke pa so bile povečane, zlasti pri študiji z večjimi odmerki. Vendar EMA ni zahtevala dodatnih eksperimentalnih toksikoloških študij. Razpoložljivi podatki so se šteli za zadostne v kombinaciji s kliničnimi preskušanji, v katerih je bilo treba oceniti celotno formulacijo (modRNA in LNP).”
Torej so bili celo v študijah na živalih ugotovljeni neželeni učinki – kljub temu pa Cooke lažno trdi, da “ni bilo varnostnih težav”
Cooke v nadaljevanju zapiše: ” V nadaljnjem pismu, poslanem 31. marca 2023, me je gospod Roos tudi prosil, naj pojasnim, kako lahko cepiva COVID-19 veljajo za varna in učinkovita za novorojenčke, ženske v rodni dobi, nosečnice in njihove otroke, če učinki na plodnost niso bili pregledani, saj so bile te skupine izključene iz kliničnih preskušanj.“
V odgovoru se sklicuje na zelo pomanjkljive in pristranske opazovalne študije“65.000 nosečnic …, ki zagotavljajo potrebna zagotovila o varnosti tega cepiva v tej populaciji“
O pomanjkljivostih teh opazovalnih študij nosečnosti in omejujočih dejavnikov, ki jih omejujejo, sem da pisal. Na primer, od 10.000 nosečnic, ki so bile dejansko cepljene iz skupine 65.000 nosečnic – jih je le 1,7 % prejelo cepivo mRNA v prvem trimesečju.
Druga pomembna dejstva, ki jih Cooke o teh študijah zamolči, so: niso bile neodvisno preverjene; prav tako niso bile randomizirane kontrolne študije – kar je zlati standard vsakega preskušanja.
Kje so podatki na ravni bolnikov iz teh 65.000 zapisov?
Ali je agencija EMA preverila 65.000 zapisov o bolnikih ali pa samo verjame na besedo avtorjev, Lipkinda in drugih?
Vsi so povezani s farmacevtsko industrijo. Heather Lipkind je na primer članica odbora za spremljanje varnosti podatkov cepiva COVID-19 v nosečnosti družbe Pfizer. Kimberly Vesco je razkrila, da prejema institucionalno podporo družbe Pfizer. Candace Fuller je razkrila, da prejema institucionalno financiranje raziskav od podjetij Pfizer in Johnson & Johnson.
Cooke prav tako ne omenja zaskrbljujočih podatkov iz predklinične študije DART – Razvojna in reproduktivna toksikologija (Developmental and Reproductive Toxicology), ki jo je družba BioNTech izvedla na podganah in ki je pokazala povečano stopnjo splavov (predimplantacijske izgube)! Glej posnetek zaslona s strani 55 poročila o nekliničnem ocenjevanju, ki ga je pripravila TGA.
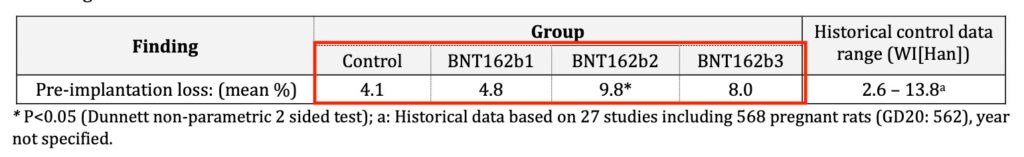
- Ugotovitve SKUPINE Zgodovinski podatki kontrole (WI[Han])
- Izguba pred implantacijo: (povprečni %) Kontrola BNT162b1 BNT162b2 BNT162b3
- 4.1 4.8 9.8* 8.0 2.6-13.8
- *P<0,05 (Dunnettov neparametrični dvostranski test); a: Zgodovinski podatki na podlagi 27 študij, ki so vključevale 568 brejih podgan (GD20: 562), leto ni navedeno.
Opazite več kot podvojeno stopnjo izgube pred implantacijo v skupini s cepivom BNT162b2 (cepivo mRNA podjetja Pfizer in BioNTech), ki je znašala 9,8 % v primerjavi s kontrolno skupino, ki je znašala 4,1 %.
Ta študija je bila dejansko kritizirana v tekočem preglednem poročilu CHMP, ki ga je novembra 2020 pripravila agencija EMA. Ocenjevalci so želeli, da družba BioNTech utemelji izbiro podgane “kot relevantne živalske vrste(prenos protiteles v placento pri glodavcih v drugem delu nosečnosti se ne šteje za podoben prenos človeških protiteles v tretjem trimesečju nosečnosti)”

b. V zvezi s študijo DART se zahteva utemeljitev zasnove študije, da se določi vrednost te študije za oceno razvojnega tveganja pri ljudeh. Predvsem bo treba upoštevati izbiro podgane kot ustrezne živalske vrste (prenos protiteles v placento pri glodavcih v drugem delu nosečnosti ni podoben prenosu protiteles pri ljudeh v tretjem trimesečju nosečnosti) in zasnovo režima odmerjanja, ali bo to privedlo do zadostnega prenosa protiteles med dojenjem, kar je enakovredno izpostavljenosti v tretjem trimesečju pri ljudeh) (NL-MS).
Če se vrnemo k Roosovemu vprašanju:“kako se lahko cepiva COVID-19 štejejo za varna in učinkovita za novorojenčke, ženske v rodni dobi, nosčnice in njihove otroke?”
Saj niso.
Šele pred kratkim sem našel obtožujoč 8-stranski dokument, ki je bil ta mesec objavljen kot del Pfizerjevega odredbe sodišča o izpisu podatkov: Pfizerjev kumulativni pregled nosečnosti in dojenja (neželenih učinkov) iz začetka leta 2021. Zaskrbljujoče ugotovitve, ki jih najdemo v moji analizi, si lahko preberete tukaj.
Iz njega so razvidni dokazi o škodljivosti za plod, ki je bil cepivu izpostavljen transplacentarno, in škodljivosti za dojenčke, ki so bili cepivu izpostavljeni po transmaternalni poti (prek materinega mleka cepljenih mater).
Študija Hanne in drugih je pokazala prisotnost mRNA cepiva COVID-19 v materinem mleku.
Vse te obremenjujoče podatke so FDA in drugi regulatorji, vključno z EMA, poznali približno v istem času (v začetku leta 2021), tik preden so ga zdravstveni organi začeli vsiljevati nosečnicam in doječim ženskam tisto pomlad.
Poleg tega je moja nedavna analiza periodičnega posodobljenega poročila EU o varnosti (PSUR#1) za organizacijo Children’s Health Defense Europe prav tako pokazala zaskrbljujoče podatke, znane od poletja 2021.
Spodaj je posnetek zaslona, ki razkriva pregled podatkov iz prvih šestih mesecev leta 2021.

- 327 827 poročil o primerih (posamezniki), ki vsebujejo 1 172 887 dogodkov (neželeni dogodki)
- Trikrat več primerov, o katerih so poročale ženske, kot primerov, o katerih so poročali moški
- Največje število prijavljenih primerov v starostni skupini od 31 do 50 let
- Tretjina vseh poročil o primerih je bila razvrščena kot resna
- 44 % poročil o primerih je bilo razvrščenih z neznanim ali nerešenim izidom
- 84 % poročil o primerih ni imelo spremljajočih bolezni
- 5115 smrtnih primerov se je zgodilo po uporabi cepiva
- 46 % primerov s smrtnim izidom se je zgodilo pri osebah brez spremljajočih bolezni
Na koncu Cooke zapiše: “Agencija EMA bo še naprej pozorno spremljala varnost cepiva COVID-19. Vse nove ugotovitve, ki bi se morale pojaviti v prihodnosti, bodo natančno analizirane in če bodo potrjene, bodo ustrezne in takojšnji ukrepi.”
Res, gospa Cooke? V to močno dvomim.
Posebna zahvala Dr. Davidu Wisemanu, Mariji Gutschi in znanstvenemu strokovnjaku, ki želi ostati anonimen.
Prvotno objavljeno na portalu Sonia Elijah Investigates
Suggest a correction