Dovezi surprinzătoare sugerează că BioNTech/Pfizer a falsificat date cheie și alte scandaluri (partea 2)

Inițial publicat pe Trial Site News
Partea 1 a raportului meu de investigație publicat în Trial Site News, s-a axat pe „Western Blots” Pfizer-BioNTech cu aspect neobișnuit – scandalul cunoscut sub numele de Blotgate. Western Blots au fost efectuate de BioNTech pentru a dovedi fidelitatea produsului lor (față de autoritățile de reglementare) că doar proteina spike așteptată era exprimată in vitro de ARNm vaccinal modificat și că era consecventă între diferitele loturi.
Problema cu faptul că acestea nu arată ca niște Western blot-uri autentice/convenționale, ci mai degrabă ca versiuni generate pe calculator (Western blot-uri automatizate, deși nu au fost etichetate ca atare în niciunul dintre rapoarte), este o distragere a atenției de la adevăratul scandal în cauză: dovezile, care arată, la prima vedere, că BioNTech/Pfizer au „copiat și lipit” aceste benzi, cu alte cuvinte, au falsificat datele lor cheie. Aceste benzi occidentale aparent fabricate (prezentate mai jos) au fost expuse în răspunsul Pfizer la întrebările Administrației pentru Alimente și Medicamente din SUA în jurul lunii noiembrie 2020, în perioada premergătoare autorizării de utilizare de urgență.
Numai atunci când aceste benzi au fost cuantificate cu ajutorul analizei software-ului de imagine (datorită unui expert anonim), munca de „copy and paste”, efectuată pe 4 loturi separate ale produsului lor, transfectat la 6 concentrații diferite, a devenit izbitor de vizibilă.
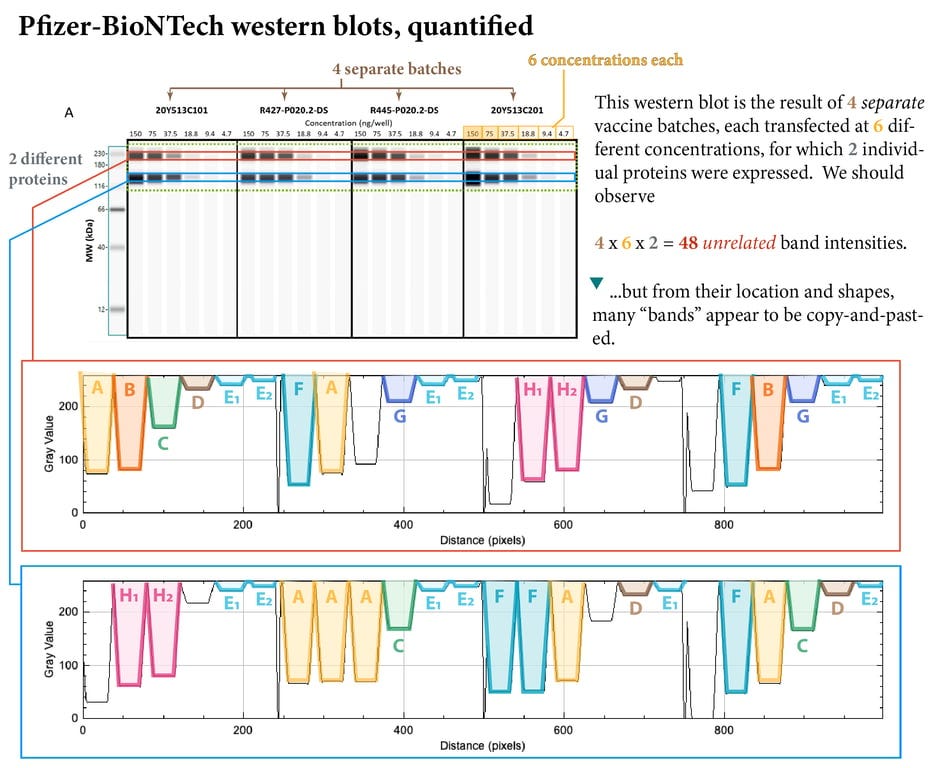
Șansele ca exact aceleași benzi să apară în mod natural în patru loturi separate de vaccin, transfectate la 6 concentrații diferite, pot fi observate în tabelul de mai jos.
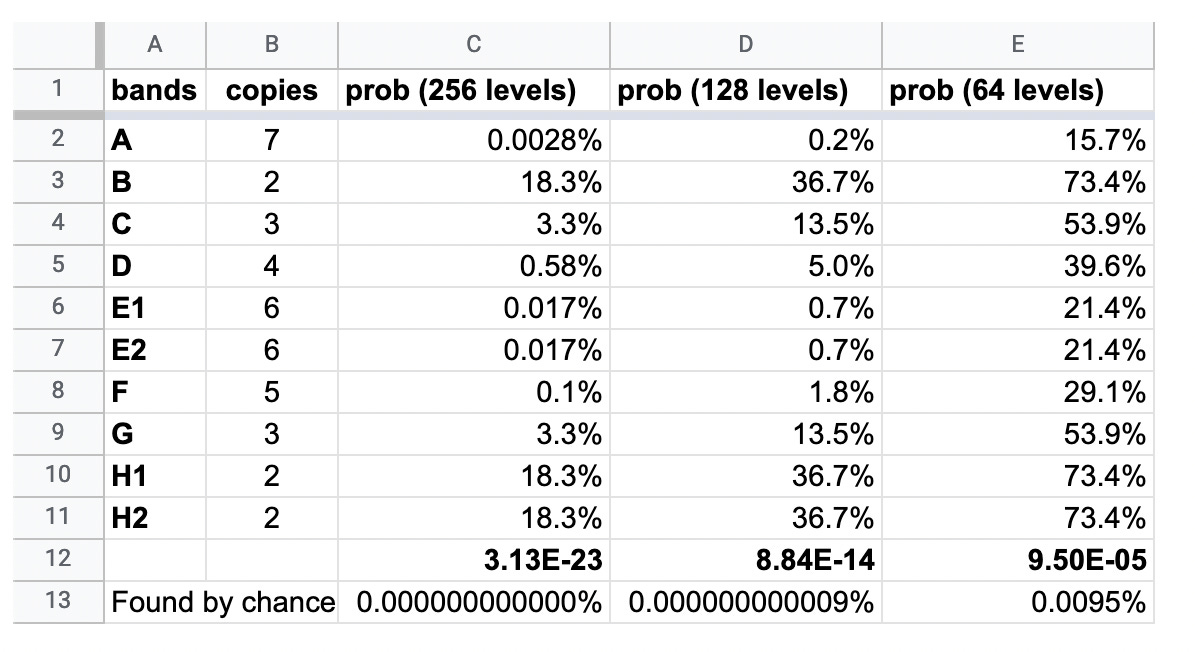
Pe urmele părții 1 a raportului meu de investigație, Epoch Times a efectuat propria investigație privind Blotgate; problemele de calitate ale ARNm ale vaccinului Pfizer-BioNTech și a făcut referire la investigația Trial Site News privind scurgerile de e-mailuri și documente ale Agenției Europene pentru Medicamente (EMA).
„Ascunderea benzilor murdare”- o privire suplimentară asupra Blotgate
La 13 ianuarie, la scurt timp după izbucnirea scandalului Blotgate, lucrarea sponsorizată de Pfizer și BioNTech, Patel et al. intitulată „Characterization of BNT162b2 mRNA to Evaluate Risk of Off-Target Antigen Translation” (Caracterizarea ARNm BNT162b2 pentru a evalua riscul de traducere a antigenului în afara țintei ) a fost publicată pe în Journal of Pharmaceutical Sciences. Lucrarea prezintă multe anomalii și merită menționat faptul că biologul computațional și molecular, Dr. Jessica Rose, a scris o analiză critică cuprinzătoare a acestui studiu.
În primul rând, merită să remarcăm interesele concurente ale autorilor, care pot fi văzute mai jos.

La discuția cu Dr. Jessica Rose, care a efectuat în mod extensiv Western Blots convenționale, aceasta a explicat: „După părerea mea de expert, [un Western tradițional] este unul dintre testele de bancă care reprezintă o procedură, precum testele de siguranță pentru produsele biologice (care ar trebui să dureze 10 ani). Un Western Blot necesită o secvență de pași specifici, acești pași nu pot fi grăbiți și nu se pot suprapune… experimentele realizate cu ajutorul Robo Jess [mașină automată Western Blot] și blot-urile prezentate de Pfizer trebuie să fie reproduse de mâini umane, reproductibilitatea este o cerință, mai ales când lista de conflicte de interese este atât de lungă din partea autorilor care le-au prezentat [Patel et al.]””
Imaginea de mai jos, preluată din lucrarea lui Patel et al. arată „Western Blot” al acestora Observați benzile regulate negre foarte groase (omogene), fără nici un fel de frotiuri.
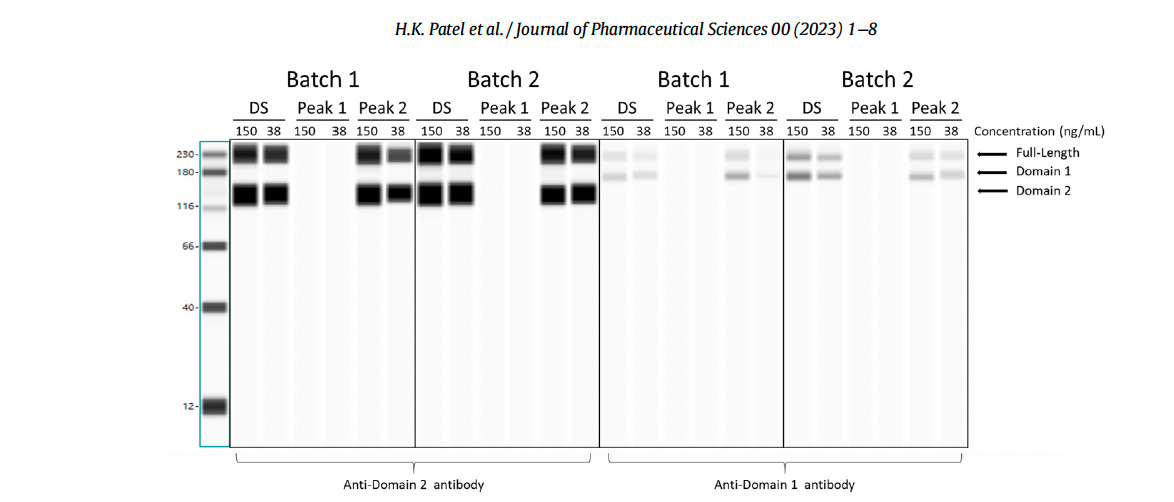
Același „Western Blot” (văzut mai jos), doar că o versiune mult mai crudă, scanată în copie, poate fi găsită în raportul redactat al Agenției Europene pentru Medicamente CHMP (Comitetul pentru Medicamente de Uz Uman) din august 2021, cu aproximativ 18 luni înainte de lucrarea lui Patel et al.
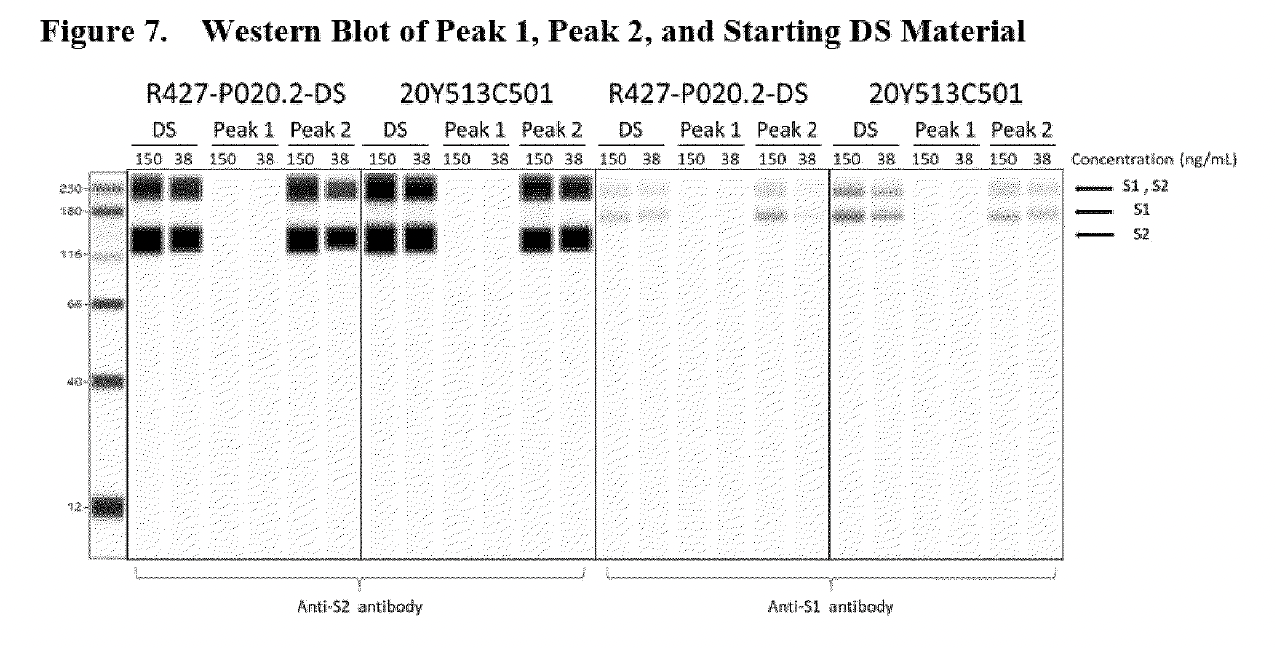
Deoarece autorii Patel et al. fac referire la tehnologia ProteinSimple în studiul lor (extras mai jos), se poate face o comparație cu o mostră de Western Blot automatizat, utilizând software-ul aceleiași companii.
‘Celulele lizate au fost analizațe cu anticorpii specifici pentru a detecta proteinele spike ale SARS-CoV-2 folosind tehnologia ProteinSimple. au fost utilizate 12-230 kDa Wes Separation Module și 25 de cartușe capilare. S-au folosit anticorpi de șoarece SARS-CoV-2 Spike S1 subunitate (R&D systems, nr. de catalog MAB105403) și anticorpi de șoarece SARS-CoV-2 Spike S2 subunitate (R&D systems, nr. de catalog MAB10557). rezultatele probelor de ARNm sunt raportate ca imagini ale benzilor de rulare a testului ProteinSimple Wes
Sursa: Lucrarea lui Patel et al
Imaginea de mai jos reprezintă un Western automatizat folosind tehnologia ProteinSimple.
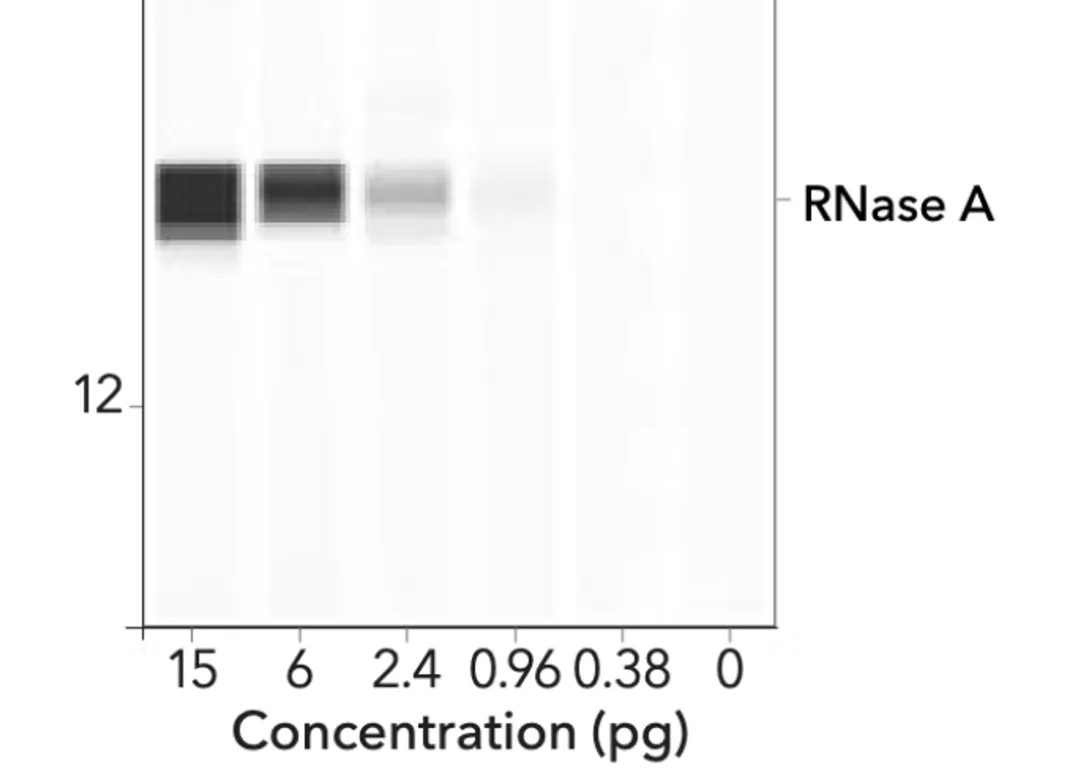
Ceea ce este izbitor este faptul că se poate observa un gradient (efect pătat) în fiecare dintre benzile variate. Acestea arată destul de diferit față de benzile negre groase și omogene ale BioNTech/Pfizer.
Pentru a obține mai multe informații, l-am intervievat pe Kevin McKernan, liderul departamentului de cercetare și dezvoltare al Proiectului Genomului Uman și om de știință în domeniul genomicii, care a explicat că „datele BioNTech/Pfizer sunt inutilizabile” și că raționamentul său pentru aspectul neobișnuit al benzilor Western Blot (observat în raportul EMA și în lucrarea Patel) se datorează faptului că „ei [BioNTech] au mărit foarte mult câștigul și majoritatea oamenilor fac acest lucru pentru a ascunde „benzile murdare” Probabil că sunt 5 benzi acolo [într-o singură bandă groasă care pare unică]” Mă refer la acest interviu informativ, mai târziu în acest raport.
Acest lucru ridică întrebarea: BioNTech/Pfizer a efectuat o mușamalizare intenționată a rezultatelor lor „Western blot” prin prezentarea unor versiuni manipulate (de Western-uri automate) autorităților de reglementare? Poate că a fost vorba de o muncă de copiere și lipire pentru FDA și de o manipulare a nivelurilor de saturație pentru EMA? Și, mai important: cum au acceptat autoritățile de reglementare aceste „Western blot” ca dovadă principală pentru a demonstra fidelitatea și consistența produsului BioNTech și Pfizer?
Am contactat EMA pentru a primi un răspuns cu privire la preocupările ridicate în cadrul acestei investigații. Ofițerul lor de presă a răspuns cu următoarea declarație: „Aceste cifre [imagini Western Blot] au fost extrase din dosarul depus și inserate în raportul de evaluare, ceea ce a dus la o pierdere a calității imaginii. În plus, software-ul de redactare utilizat de EMA pentru a pregăti documentele pentru publicare în urma unei solicitări ATD are un impact asupra rezoluției documentelor.
În ceea ce privește validarea metodelor, metodele analitice Western Blot utilizate în studiile de caracterizare au fost evaluate anterior în timpul cererii inițiale de autorizare de introducere pe piață condiționată, ca parte a „istoriei dezvoltării și evaluării comparabilității” și au fost considerate adecvate în acest scop
FDA, Pfizer și BioNTech nu au răspuns pentru comentarii.
Parametrii de calitate stabiliți la câteva luni după ce a fost acordată autorizația de punere pe piață
Motivul pentru care deținătorul autorizației de introducere pe piață (BioNTech) a efectuat o serie suplimentară de teste a fost acela că autorizația de introducere pe piață condiționată (CMA) a fost acordată pe baza îndeplinirii de către deținătorul autorizației de introducere pe piață a unor obligații specifice (cum ar fi date suplimentare pentru a caracteriza în continuare speciile de ARNm trunchiat și modificat) impuse de EMA. Până la momentul acordării AMC, mai multe probleme de CMC (chimie, fabricație și control) au fost semnalate ca fiind motive de îngrijorare majoră de către EMA, în special scăderea integrității ARNm (prezența ARNm trunchiat/fragmentat – lipsit de un atribut critic,la capătul 5′ și/sau coada poli(A)) din loturile comerciale în comparație cu cele utilizate în studiile clinice. „Soluția” la această problemă majoră a fost reducerea criteriilor de acceptare a speciilor de ARNm fragmentate/trunchiate până la 50%, la care autoritățile de reglementare au renunțat pur și simplu.
Farmacistul canadian, Maria Gutschi, PharmD, care are peste 30 de ani de experiență în spital, în comunitate și în guvern, a analizat în mod independent problemele de calitate ale vaccinului Pfizer/BioNTech identificate de Agenția Europeană pentru Medicamente, într-o prezentare video informativă. Vorbind cu Gutschi, aceasta a ridicat alte preocupări importante: ‘Abia în mai 2021 [la 5 luni după ce a fost acordată autorizația], OCABR a stabilit parametrii de calitate și, mai ales, standardizarea testelor utilizate. O problemă pe care am constatat-o a fost că, la lansare, multe dintre testele utilizate pentru a determina calitatea și identitatea erau teste ‘in house’ de către BioNTech. Ei bine, un organism de reglementare nu poate accepta așa ceva. Acestea trebuie validate astfel încât să fie consecvente, reproductibile și fiabile‘
OCABR este acronimul de la Official Control Authority for Batch Release (Autoritatea oficială de control pentru eliberarea loturilor), care stabilește liniile directoare pentru vaccinurile umane autorizate în UE. Observați data de mai 2021 evidențiată în documentul OCABR, văzut mai jos.

Faptul că OCABR a stabilit primii parametri de calitate pentru un vaccin uman, la un interval de timp uimitor de 5 luni după ce a fost acordată CMA- este fără precedent. În al doilea rând, faptul că aceste teste (teste) trebuiau să fie validate este demn de remarcat.
Testele „interne” discutabile
Este demn de remarcat faptul că îngrijorarea lui Gutschi cu privire la testele „in-house” ale BioNTech a fost împărtășită și de un evaluator EMA în Raportul de revizuire continuă al raportorului din noiembrie 2020, care a făcut obiectul unor scurgeri de informații, cu puțin timp înainte de acordarea CMA.

Revenind la documentul de orientare din 2016 al FDA privind „Integritatea datelor și conformitatea cu CGMP„, acesta precizează: ” Integritatea datelor și conformitatea cu CGMP: „În ultimii ani, FDA a observat din ce în ce mai multe încălcări ale CGMP care implică integritatea datelor în timpul inspecțiilor CGMP. Acest lucru este îngrijorător, deoarece asigurarea integrității datelor este o componentă importantă a responsabilității industriei de a asigura siguranța, eficacitatea și calitatea medicamentelor și a capacității FDA de a proteja sănătatea publică”
Considerarea de către FDA a încălcărilor integrității datelor ca fiind „îngrijorătoare” pare să dispară – prin acceptarea cu ușurință a datelor aparent „copiate și lipite” ale BioNTech. Poate că pentru ei a fost doar un exercițiu de bifare a unei căsuțe, pentru a părea că își fac diligențele necesare pentru „protejarea sănătății publice”
Benzile „neașteptate” care apar în Western blot-urile autentice ale BioNTech
Printre toate „Western blot-urile” generate pe calculator, BioNTech a prezentat de fapt două Western-uri autentice (al doilea va fi discutat mai târziu), ceea ce a dovedit că știau cum să le facă. În raportul de evaluare „Rolling Review” al raportorului EMA, care a făcut obiectul unor scurgeri de informații, au fost formulate următoarele critici la adresa studiului 20-0211 al BioNTech „cu privire la rezultatele obținute prin Western Blot”, notate mai jos.

În luna februarie a anului trecut, studiul 20-0211 (studiul specificat mai sus) efectuat de BioNTech a fost publicat ca parte a descărcării de date Pfizer ordonată de instanță. Western Blot-ul autentic extrem de revelator prezentat în acel studiu poate fi văzut mai jos.

Din raportul de evaluare al EMA din noiembrie 2020, știm că agenția a semnalat greutățile moleculare neașteptate (măsurate în kDa) ale celor două benzi proteice prezentate în testul Western Blot, de 190kDa și, respectiv, 100 kDa, ceea ce a determinat-o să ceară o explicație de la BioNTech. Acum, proteina spike completă are o greutate moleculară de 141 kDa, iar S1 (subunitatea proteinei spike) are o greutate moleculară de 76,5 kDa, care a fost utilizată ca martor. Observați, din figura de mai sus, că nu există benzi proteice la niciuna dintre aceste greutăți moleculare așteptate în banda BNT 162B2 și că greutatea moleculară așteptată de 76,5 kDa a proteinei S1 nu a fost observată în banda de control S1. Aceste anomalii au ieșit în evidență pentru autoritatea de reglementare, dar, cumva, dezvoltatorul vaccinului, BioNTech, care ar fi cunoscut cu siguranță greutatea moleculară așteptată a proteinei spike complete, deoarece produsul său ARNm ar trebui să o codifice, nici măcar nu le-a recunoscut.
Pentru a exacerba eșecul lor complet în abordarea acestor probleme, BioNTech a scris o descriere extrem de inexactă a Western Blot-ului lor – de fapt, exact opusul a ceea ce era arătat în imagine: „BNT162b2b2 are o dimensiune preconizată de 141,14 kDa” și „proteina subunității S1 a SARS-CoV-2 (76,5kDa) a fost utilizată ca și control pozitiv„
Acest lucru sugerează că, probabil, este posibil ca proteina de vârf S1S2 să nu fi fost exprimată de ARNm modificat vaccinal sau, dacă a fost, poate că au fost exprimate și alte proteine aberante, care provin din molecule de ARN fragmentate/trunchiate în substanța medicamentoasă.
Lipsa secvențierii genomului și problemele legate de N1 Metilpseudourină
Când a fost interogat cu privire la problemele legate de calitatea vaccinului Pfizer-BioNTech, cercetătorul în genomică, Kevin McKernan, a dat următorul răspuns:
„Nu avem nicio secvențiere a ADN-ului pe aceste loturi. Este o nebunie absolută! Venind de la proiectul genomului uman, publicam o secvență la fiecare 24 de ore pentru a ne asigura că lumea are acces la cele mai recente date care provin din proiectul genomului uman. Să trecem rapid la ziua de azi și nu puteți găsi nicio secvențiere a genomului loturilor„
Este uimitor faptul că autoritățile de reglementare s-au bazat pe aceste teste Westerns blot cu aspect manipulat de la BioNTech, în loc să solicite secvențe genomice ale loturilor, pentru a dovedi consistența și fidelitatea acestora.
McKernan a continuat să se refere la problemele cauzate de ARN-ul modificat sintetizat folosind o bază modificată: „Avem un produs ARNm în care fiecare uridină a fost înlocuită cu N1 Metilpseudourină, pe care organismul nu a mai văzut-o niciodată. Ei [BioNTech și Pfizer] au ales codoni de oprire care sunt cei mai cunoscuți pentru crearea de erori. Ei [erau conștienți de problemă, dar nu au rezolvat-o în mod corespunzător. Acest lucru înseamnă că atunci când ribozomii se duc să citească șablonul, sunt foarte confuzi, deoarece nu l-au mai văzut niciodată înainte.”
McKernan a scris împreună cu Dr. Peter McCullough și Anthony Kyriakopoulos o lucrare intitulată „Differences in Vaccine and SARS-CoV-2 Replication Derived mRNA: Implicații pentru biologia celulară și boala viitoare” Autorii au concluzionat că „modificările codonilor sinonimici încorporați în vaccinurile ARNm pot modifica conformația preconizată a proteinei codificate, deoarece viteza și eficiența traducerii pot duce la o pliere diferită a proteinei… Strategiile de optimizare a codonilor pentru dezvoltarea vaccinurilor ARNm pot duce la deregularități imunitare, pot afecta reglarea epi-transcriptomică și pot duce la progresia bolii„
Uridina modificată (N1 metilpseudorină) a fost încorporată în ARNm pentru a eluda răspunsul imunitar înnăscut și a promova traducerea proteinei. Cu toate acestea, în raportul Rolling Review al EMA din noiembrie 2020 (pagina 61), a fost ridicat un potențial risc de siguranță cu ARN modificat (modRNA), a se vedea mai jos.
‘MODARN conține o substituție a 1-metil-pseudouridinei cu uridină. Această substituție diminuează recunoașterea ARN-ului vaccinal de către senzorii imunității înnăscute. Cu toate acestea, nu a fost furnizată nicio discuție suplimentară cu privire la riscul răspunsurilor autoimune induse de modRNA. Solicitantul este invitat să discute în continuare posibilitatea ca vaccinul cu ARNm să poată declanșa potențiale răspunsuri autoimune și cum intenționează să evalueze eventuala apariție a acestora.
Nu se știe dacă BioNTech a evaluat vreodată potențialul risc de siguranță al răspunsului autoimun cauzat fie de uridina modificată, fie de proteinele traduse (altele decât proteina spike), deoarece până în august 2021, cu data limită de iulie 2021 a trecut, încă nu s-a făcut acest lucru. (A se vedea instantaneul de mai jos, pagina 13 din raportul CHMP al EMA din august 2021)

Ceea ce este deranjant sunt concluziile celui mai mare studiu de acest tip de la Spitalul Universitar King Fahad din Khobar, Arabia Saudită, care leagă vaccinurile cu ARNm de declanșarea bolilor autoimune, care TrialSite tocmai a prezentat recent un raport. „Mimetismul molecular”, declarat ca fiind o preocupare în raportul EMA de mai sus, este aceeași ipoteză avansată în studiu ca fiind mecamismul asociat cu vaccinurile cu ARNm care provoacă un proces autoimunitar.
Probleme potențiale care decurg din procesul de fabricație
Figura de mai jos arată viziunea simplistă folosită pentru a promova modul de funcționare a vaccinurilor cu ARNm.
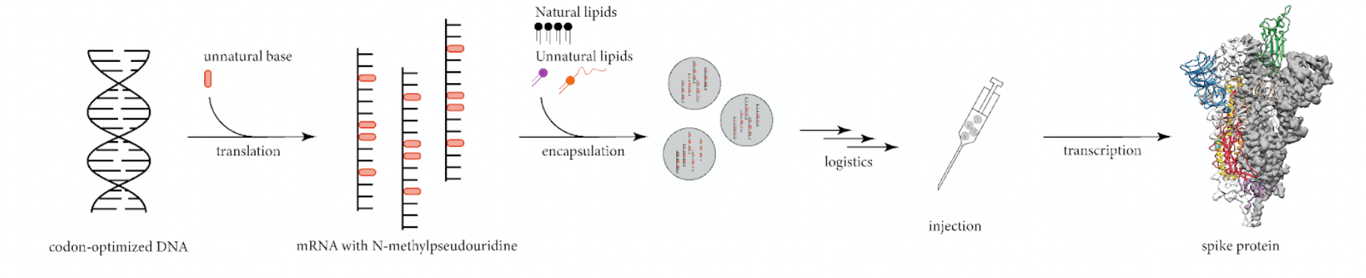
Când, de fapt, procesul este extrem de variabil, care la rândul său generează produse proteice extrem de variabile, a se vedea figura de mai jos.

Fiecare etapă a procesului de fabricație poate introduce impurități necunoscute și erori necunoscute, de la traducerea „necredincioasă” a ADN-ului optimizat pentru codon, care poate genera fragmente de ARNm (nu intacte), până la transcrierea „necredincioasă” a amestecului de ARNm în corpul uman, care poate genera produse proteice neașteptate.
McKernan a continuat să explice în continuare rata de eroare și implicațiile acesteia: ‘Estimarea mea este că există o eroare la fiecare moleculă de vaccin – având în vedere că există 14 trilioane de molecule în fiecare injecție – nu știm ce înseamnă acest lucru din punct de vedere imunologic. Acesta este motivul pentru care trebuie să existe o secvențiere lot cu lot înainte de a injecta un produs cunoscut pentru a produce proteine noi în interiorul oamenilor„
ARNm modificat în lungime completă al vaccinului Pfizer-BioNTech care codifică proteina spike are o lungime de ∼4300 nucleotide, nt. Orice cantitate mai mică este considerată o specie de ARNm fragmentată, pe care EMA a clasificat-o ca fiind o „impuritate legată de produs”. Acest lucru duce la un alt scandal, cel cunoscut sub numele de Humpgate.
Scandalul Humpgate
Humpgate poate fi privit ca precursorul lui Blotgate. În timp ce Blotgate s-a axat în principal pe benzile proteice cu aspect fals exprimate de ARNm vaccinal observate în Westerns de la BioNTech, Humpgate se referă la speciile de ARNm trunchiat semnalate de EMA și de alte autorități de reglementare. Numele provine de la „cocoașele” observate în imaginea din postarea din social media de mai jos.
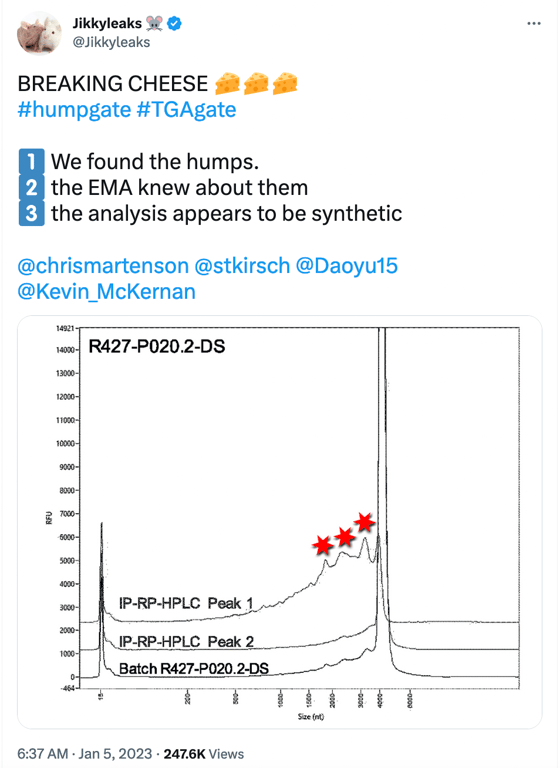
Cele 3 „cocoașe” indicate de stelele roșii reprezintă speciile de ARN trunchiat/fragmentat având o lungime scurtată (nt) <4000nt. Imaginea de mai sus reprezintă o electroferogramă Fragment Analyser (care este imaginea de sus din Figura 2 prezentată mai jos) preluată de la pagina 15 din raportul EMA redactat din vara anului 2021, pe care BioNTech l-a întreprins pentru a îndeplini SO1 (obligația specifică 1) stabilită de EMA, care a solicitat date suplimentare pentru a caracteriza mai bine speciile de ARNm trunchiat și modificat.

Au fost prelevate probe fracționate din Procesul 1(R427-P020.2-DS, lotul de studiu clinic, imaginea de sus) și Procesul 2(20Y513C501, lotul PPQ, imaginea de jos) utilizând RP-HPLC cu împerechere ionică pentru a caracteriza în continuare speciile de ARNm intacte (cu lungime completă) și fragmentate. Ambele loturi (Procesul 1 și 2) prezintă mici cocoașe care conduc la un vârf mare la o dimensiune de aproximativ 4300 nt, care reprezintă specia ARNm de lungime completă. Linia grafică etichetată ca Peak 1 arată materialul „purificat” reanalizat compus numai din specii de ARNm fragmentar (acestea sunt micile cocoașe observate în partea stângă a vârfului mare de aproximativ 4300 nt din eșantionul lotului), iar Peak 2 este materialul reanalizat „purificat” compus din specii de ARNm intacte, observate la „vârful mare”
Aceeași electroferogramă poate fi găsită în lucrarea publicată în ianuarie 2023, Patel et al. (a se vedea imaginea de mai jos, publicată la 18 luni după raportul EMA). Cu toate acestea, autorii Patel et al. își citează cercetarea ca fiind actuală, când este o versiune reelaborată a propriului răspuns al Pfizer/BioNTech la întrebările FDA și EMA de acum 18 luni. Faptul că autorii și-au prezentat studiul ca fiind „independent” și „actual”, când tehnologia ProteinSimple Wes utilizată în cercetarea lor a fost întreruptă începând cu 30 iulie 2021, este cel puțin nesincer.
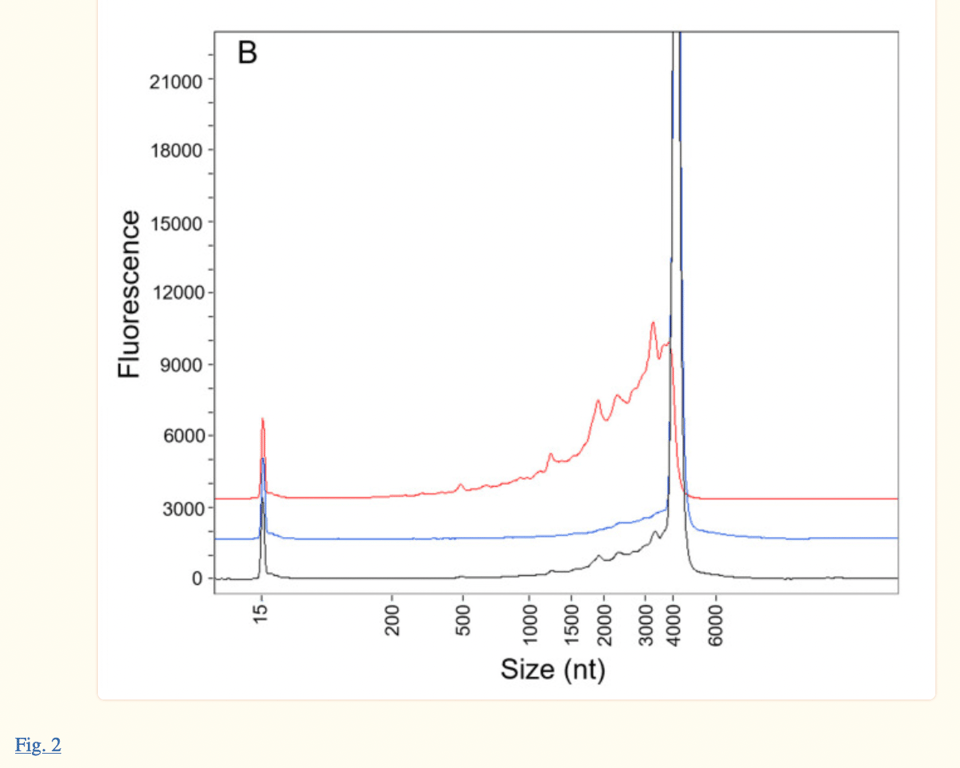
Atât lucrarea lui Patel et al., cât și documentul EMA iau în derâdere cocoașele observate în partea stângă a vârfului principal la aproximativ 4300 nt. În raportul EMA se afirmă „(Figura 2) demonstrează că Vârful 1 este format aproape în întregime din specii fragmentate, în concordanță cu datele furnizate anterior în Assessment of Response to CHMP Q01-Quality 11-Dec-2020”
Problema cu ipoteza BioNTech
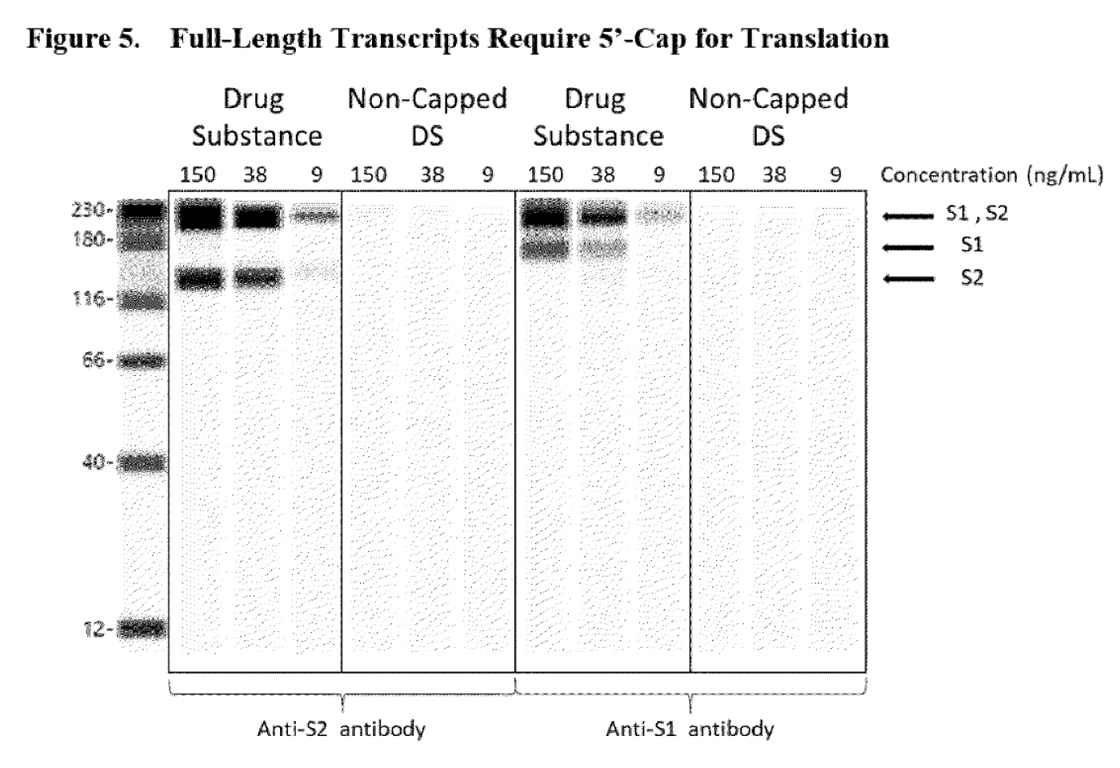
Modul în care BioNTech a asigurat EMA că aceste specii trunchiate de ARN nu ar fi capabile să susțină traducerea proteinelor, astfel încât speciile trunchiate văzute ca „cocoașe” în electroferograme nu ar fi considerate o problemă, a fost prin efectuarea de noi teste Western Blot pentru a dovedi că ARN-ul „transcripții necesită atât 5′-cap cât și poli (A) pentru a susține traducerea proteinelor…”

Iată cum arată un ARN BNT162b2 de lungime completă. La începutul transcripției ARN-ului se adaugă un capac 5′, iar la sfârșitul transcripției se adaugă o coadă poli (A) 3′. Ribozomii citesc transcriptul din direcția 5′ spre 3′.

Figurile de mai jos (6 și 5) sunt preluate din raportul CHMP al EMA din august 2021.

Liniile goale prezentate în panourile de substanțe medicamentoase non-poly(A), au fost suficiente pentru a dovedi autorității de reglementare că ARN-ul lipsit de Poly (A) nu ar fi capabil să exprime proteina S1S2 spike. Cu toate acestea, problema cu acest test este că nu confirmă faptul că orice alte proteine aberante (care a fost o preocupare inițială a EMA) ar putea fi exprimate de acest ARN trunchiat, deoarece au fost utilizați doar anticorpii de detecție specifici domeniului S1 și S2. Western Blot prezentat mai jos împărtășește aceeași problemă. Acest test a fost utilizat pentru a reasigura autoritatea de reglementare că transcriptul ARN lipsit de un 5’cap nu ar putea exprima proteina de vârf S1S2.
În plus, s-a presupus că specia de ARN fragmentat era rezultatul unor opriri premature ale transcripției sau al hidrolizei ARNm (când o moleculă se rupe în două bucăți atunci când reacționează cu apa), a se vedea extrasul de mai jos.
‘Evaluarea asociată a siguranței a arătat că probabilitatea ca speciile fragmentate să fie generate de opriri transcripționale premature sau de hidroliza ARNm. Ca atare, speciile fragmentate nu au, în mod predominant, atât elementele 5’-cap cât și coada poli (A) necesare pentru exprimarea proteinei
Sursă: Raportul CHMP al EMA din august 2021
Acest lucru a dat un sentiment fals de siguranță că un transcript trunchiat de ARNm ar putea avea doar fie un 5’cap, fie o coadă poli (A), dar niciodată ambele.
Mirajul testului de degradare
Potențialul transcriptelor trunchiate de ARN de a produce proteine a fost investigat în continuare de BioNTech la cererea autorității de reglementare. Ceea ce este interesant este că lotul (1071509) a fost selectat în mod intenționat și degradat în mod intenționat prin expunere la temperaturi ridicate, pentru a genera probe cu specii fragmentate. Western Blot-ul prezentat mai jos este al doilea tradițional prezentat de BioNTech. Acesta arată că capacitatea transcriptului de ARN (atunci când este degradat de căldură, deci fragmentat) de a exprima o proteină devine mai mică.
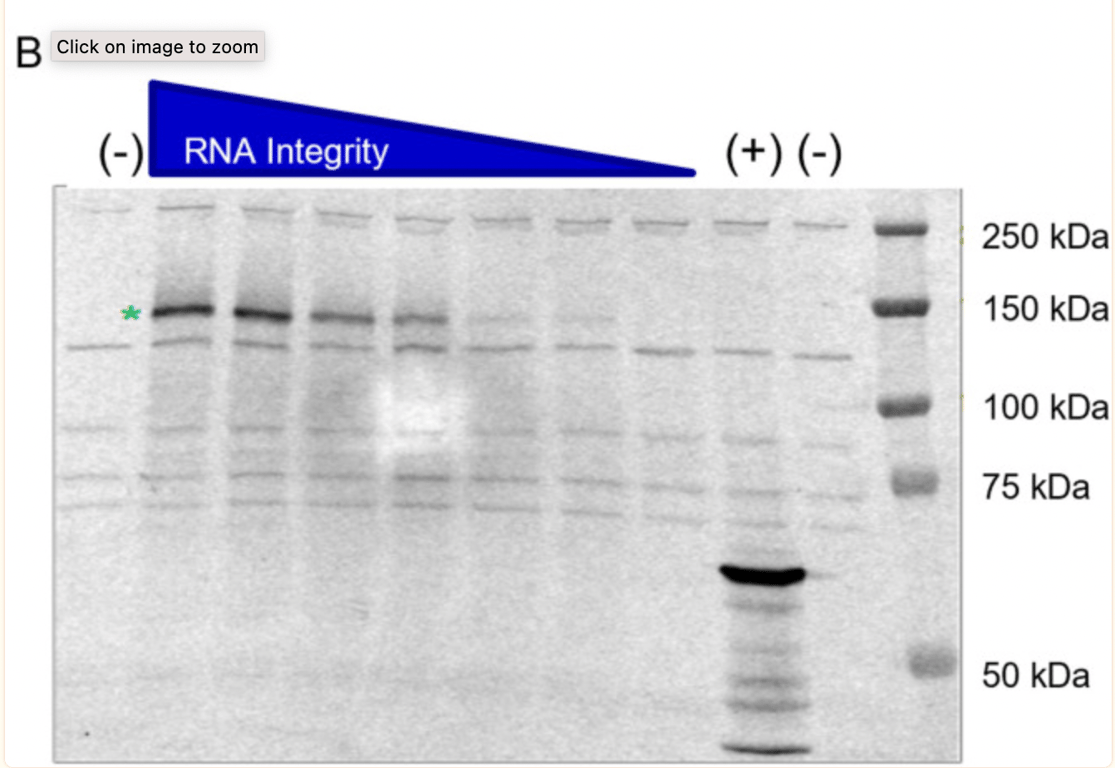
Steluța verde arată că proba BNT162b2 nedegradată (nu a fost încălzită, ARN intact/cu integritate ridicată) a produs o proteină de aproximativ 140kDa, în concordanță cu dimensiunea așteptată a proteinei S1S2 aglicozilate. BioNTech afirmă că „Nu au fost detectate specii de proteine trunchiate sau alte specii de proteine dincolo de benzile de fond observate în proba de control negativ”, însă, în banda probei nedegradate, sunt vizibile benzi de proteine și nu se oferă nici o explicație cu privire la ce sunt acestea.
În interviul acordat de McKernon, acesta a explicat: „ceea ce au făcut în studiul lor este că au luat ARNm și nu l-au fragmentat așa cum se obține în urma procesului de fabricație, ci l-au încălzit! Motivul pentru care sunt fragmentate este că polimerazele se blochează pe aceste baze non-native (modificate) în sintetizarea ARN-ului, astfel încât obțineți aceste porțiuni mai scurte de ARN în procesul de fabricație, iar acest proces variază probabil în funcție de nucleotidele pe care le obțin de la furnizorii lor”
În august 2021, raportul EMA, o nouă obligație a fost făcută pentru BioNTech de a îndeplini o solicitare pentru același exercițiu de caracterizare, care să fie făcut pentru cel puțin trei loturi suplimentare de tozinameran (ARNm modificat, substanță medicamentoasă). După cum puteți vedea, acest lucru nu a fost îndeplinit până în august 2021.

Și conform ultimei actualizări (2 februarie 2023) Comirnaty: EPAR report, această obligație a rămas în continuare neîndeplinită.

De asemenea, McKernan a făcut referire la lucrarea lui Patterson et al. care, în mod alarmant, a găsit versiuni mutante ale proteinei spike la persoanele vaccinate, care nu existau la persoanele nevaccinate care aveau COVID-19. Acest lucru poate fi considerat ca fiind date observaționale din lumea reală care arată că versiunile mutante (aberante) ale proteinei spike sunt traduse de ARNm modificat de vaccin.
În comentariul său final, McKernan a declarat: „Oamenii de reglementare dorm la volan. Au părăsit cârma și au lăsat să se meargă pe controlul de croazieră”
Nu aș putea fi mai mult decât de acord.
Publicat inițial pe Trial Site News
Suggest a correction






