La última entrega explosiva de datos condenatorios de la EMA confirma su fracaso: PSUR nº 3, los casos de embarazo y lactancia
Gracias a una solicitud de la Ley de Libertad de Información, el Informe Periódico de Actualización de Seguridad de la UE #3 (PSUR #3), que cubre el período de 6 meses de 19 de diciembre de 2021 hasta el 18 de junio de 2022, recientemente estuvo accesible en el blog austriaco de Política y Ciencia, tkp.
Mi análisis del PSUR # 1 fue publicado en Children’s Health Defense Europe, que cubría los eventos adversos reportados durante los primeros 6 meses de 2021 para la vacuna COVID-19 de ARNm de Pfizer-BioNTech. En este momento, PSUR #2 y los apéndices para PSUR #1 y #3 aún no se han publicado.
Este artículo específico es la primera parte del análisis del PSUR #3, el tercer documento de farmacovigilancia solicitado por el regulador de medicamentos de la Unión Europea, la Agencia Europea de Medicamentos (EMA), preparado por Pfizer/BioNTech y firmado por la Vicepresidenta de Medicina y Seguridad Mundial de Pfizer, Barbara De Bernardi MD, el 18 de agosto de 2022.
Resumen de los datos
- 508.351 informes de casos (individuos) conteniendo 1.597.673 eventos
- Se notificaron tres veces más casos en mujeres que en hombres
- 1/3 de todos los casos se clasificaron como graves
- 3280 muertes notificadas
- el 60% de los casos se notificaron con resultado desconocido o no recuperado
- el 92% de los casos no presentaban comorbilidades
- El mayor número de casos se produjo en el grupo de edad de 31-50 años
- Alemania registró el mayor número de casos (22,5% de todos los casos registrados en el mundo)
Este informe se centra en los casos de efectos adversos durante el embarazo y la lactancia recogidos en el explosivo informe de 396 páginas.
Casos de lactancia
Es importante señalar que tras una revisión más detallada del PSUR # 1, surgió algo extremadamente preocupante: se notificaron efectos adversos en bebés amamantados, expuestos indirectamente a la inyección de ARNm de Pfizer-BioNTech, por sus madres vacunadas. La captura de pantalla de abajo está tomada de la página 165 del PSUR #1.

El hecho de que 2 casos de los datos post-comercialización (PM) se refieran a bebés que estuvieron expuestos indirectamente a la vacuna de ARNm de Pfizer-BioNTech (BNT162b2) por vía transmamaria (a través de la leche materna) y que, en consecuencia, sufrieron un derrame cerebral (hemorragias del sistema nervioso central y accidentes cerebrovasculares), es chocante.
A continuación, en la página 149 (captura de pantalla a continuación), se registraron 3 casos más de bebés que sufrieron acontecimientos adversos neurológicos, por ejemplo, convulsiones, por estar expuestos indirectamente a la vacuna a través de la leche materna de sus madres vacunadas.

Este patrón también se observó en la PSUR #3, la captura de pantalla que figura a continuación está tomada de la página 80.

Del análisis de las dosis de refuerzo (> 2 dosis de la serie primaria), se registraron 455 casos durante el intervalo de notificación de 6 meses (1 de los datos del ensayo clínico y 454 registrados a partir de los datos posteriores a la comercialización) en bebés cuyos casos «se excluyeron debido a la exposición indirecta (transplacentaria/transmamaria) a BNT162b2»
Otro ejemplo, que se muestra en la siguiente captura de pantalla tomada de la página 239, informa de 4 casos (bebés) que sufrieron acontecimientos adversos respiratorios de interés especial (AESI), que «se determinó que no eran contributivos y no se incluyeron en la discusión ya que estos casos implicaban exposiciones a la vacuna durante el embarazo de la madre o a través de la lactancia.»

En ambos informes PSUR, Pfizer/BioNTech da la misma razón por la que estos casos «no se incluyen en la discusión» porque «se determinó que no eran contributivos» ya que involucraban a bebés «que estuvieron expuestos indirectamente a BNT162b2»
Dada la gravedad de esta importante señal de seguridad que afecta a los bebés lactantes, pasar por alto el hecho de que los casos de efectos adversos de estos bebés no fueron contributivos porque estuvieron expuestos indirectamente a la vacuna a través de la leche materna es inconcebible.
En los resultados de un estudio pionero realizado en septiembre de 2022 por Hanna et al. y publicado en JAMA Paediatrics, los investigadores hallaron trazas de ARNm de la vacuna COVID-19 en la leche materna de mujeres lactantes, tan pronto como una hora después de la vacunación. Llegaron a afirmar: «Especulamos que, tras la administración de la vacuna, las nanopartículas lipídicas que contienen el ARNm de la vacuna son transportadas a las glándulas mamarias por vía hematógena y/o linfática»
Recuerde la afirmación inquebrantable, aunque completamente infundada, de los reguladores de medicamentos y las autoridades sanitarias de todo el mundo de que la vacuna de ARNm simplemente se queda en el brazo. Pues bien, eso no podría estar más lejos de la realidad.
En la reciente carta filtrada de la Directora Ejecutiva de la EMA, Emer Cooke, a la Presidenta del Comité Especial COVID-19, la eurodiputada Kathleen Van Brempt, Cooke admitió a regañadientes «que las nanopartículas lipídicas pueden distribuirse de forma bastante inespecífica a varios órganos como el hígado, el bazo, el corazón, el riñón, el pulmón y el cerebro, siendo el hígado el órgano donde las nanopartículas lipídicas parecen distribuirse más «
Su admisión se produjo a raíz del informe de evaluación de la Therapeutics Goods Administrations (TGA) de Australia sobre el estudio no clínico de biodistribución de Pfizer, planteado por el eurodiputado Robert Roos en la audiencia del Comité Especial sobre COVID-19 celebrada el 27 de marzo de 2023. El informe de enero de 2021 de la TGA, reveló de forma alarmante que las nanopartículas lipídicas que encapsulan el ARNm, viajan al hígado, bazo, cerebro, ojos, médula ósea, glándulas suprarrenales, ovarios y testículos – casi todos los tejidos orgánicos.
Los casos de embarazo (datos acumulados de los ensayos clínicos)
Los casos de embarazo que surgen de los datos acumulados de los ensayos clínicos en PSUR# 3, se originaron en los ensayos clínicos de fase 1/2/3 de Pfizer hasta junio de 2022. Aunque las mujeres embarazadas fueron excluidas del ensayo pivotal de Pfizer, algunas de las participantes quedaron embarazadas. Como parte de la carta de aprobación para el uso de emergencia de COMIRNATY (nombre comercial de la vacuna de ARNm de Pfizer-BioNTech), la Organización Mundial de la Salud (OMS) solicitó que BioNTech, titular de la autorización de comercialización, supervisara sus resultados.
Se notificaron 697 casos acumulados de embarazo, que comprendían 597 casos de la madre y 100 casos del bebé/feto. en ‘431 casos se notificó la exposición a la vacuna in utero sin que se produjera ningún evento clínico» en los casos de la madre. A continuación se desglosan los 166 casos de madres que sí notificaron acontecimientos clínicos adversos. Los números entre paréntesis reflejan el número de acontecimientos notificados con frecuencia.
- ~ 1/5 de todos los casos de madres notificaron acontecimientos adversos graves (139)
- abortos espontáneos (46)
- Preeclampsia (7)
- Desproporción cefalopélvica (6)
- Aborto fallido, muerte fetal, hemorragia posparto, separación prematura de la placenta (4 cada una)
- Amenaza de aborto, embarazo ectópico, hipertensión gestacional, parto prematuro, trabajo de parto prematuro (3 cada uno)
- Aborto incompleto, hiperémesis gravídica, exposición materna a través de la pareja durante el embarazo, aborto espontáneo de la pareja, trastorno uterino (2 de cada)
- COVID-19 (9)
- Anemia (2)
De la lista anterior, merece la pena señalar que «exposición materna a través de la pareja durante el embarazo» y «aborto espontáneo de la pareja» se refieren a casos de mujeres expuestas indirectamente al BNT162b2 por sus parejas vacunadas. Esto se relaciona de manera importante con la diseminación de la vacuna, que estaba en el radar de Pfizer incluso antes de que comenzara su ensayo clínico, pero que más tarde se informó ampliamente al público como un mito. Según el propio protocolo del ensayo clínico de Pfizer, los casos de mujeres embarazadas expuestas indirectamente a la vacuna por sus parejas (que participaron en el ensayo) se clasificaron como «exposición durante el embarazo» y se notificaron inmediatamente a Pfizer Safety en el formulario de efectos adversos graves de la vacuna en un plazo de 24 horas desde que el investigador tuvo conocimiento de ello. El investigador debía realizar un seguimiento del embarazo y notificar el resultado a Pfizer Safety.
Los casos del bebé/feto (datos acumulados del ensayo clínico)
Lo inquietante es que 98 de los 100 casos de bebés/fetos se consideraron graves. Las siguientes capturas de pantalla reflejan sus terribles resultados.

Para los 68 casos de bebés/fetos que mostraron «nacido vivo sin anomalía congénita», los resultados de los efectos adversos graves pueden leerse en la siguiente captura de pantalla.

También hubo un caso de mortinato sin anomalía fetal durante el periodo de notificación, que se codificó como síndrome de distrés respiratorio neonatal.
Los casos de embarazo (de los datos posteriores a la autorización)
Según los datos posteriores a la autorización, se produjeron 3.642 casos de embarazo con 1.898 resultados de embarazo durante el periodo de notificación (diciembre de 2021 a junio de 2022). Alemania tuvo el mayor número de casos de embarazo (837) en el periodo de notificación, seguida del Reino Unido con 475 casos. La tabla de esos 1898 resultados puede verse a continuación.
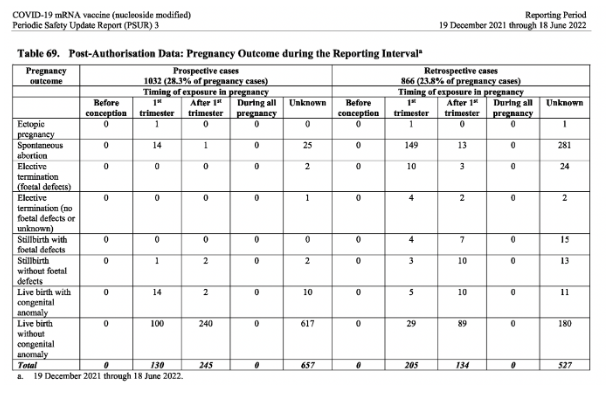
Resulta significativo que un tercio de los resultados de embarazo proporcionados durante el periodo de referencia fueran negativos.
Aborto espontáneo: 483
Nacidos vivos con anomalías congénitas: 52
Nacidos muertos con defectos fetales: 26
Interrupción electiva del embarazo (por defectos fetales): 39
De los 3.642 casos de embarazo, 322 se clasificaron como casos de bebé/feto y 3.320 como casos de madre.
Los casos de bebé/feto (datos posteriores a la autorización)
El 90% de los 322 casos de bebé/feto se clasificaron como graves. Hubo 39 casos de «nacido vivo con anomalía congénita» Las capturas de pantalla siguientes muestran la aterradora variedad de esos defectos.

Hubo 37 casos de aborto espontáneo en los casos de bebés con «restricción del crecimiento fetal (18), anomalía congénita (8), frecuencia cardiaca fetal anormal (3), anomalía citogenética, mala perfusión vascular fetal (2 en cada caso)»
En 4 casos, la madre tenía antecedentes médicos subyacentes, pero en los 33 restantes, según el informe, «había poca información sobre los antecedentes obstétricos o la medicación de la madre, lo que impedía evaluar la causalidad»
Se notificaron 23 casos de interrupción electiva del embarazo. En 22 de los 23 casos «se informó de interrupción electiva debido a defectos fetales» Hubo otros 21 casos de mortinatos, de los que algo más del 70% presentaban defectos fetales.
En marcado contraste con los datos condenatorios, el informe concluye: «De la revisión de estos casos no se desprende ninguna señal de seguridad en relación con el uso en mujeres embarazadas o lactantes..»
Además, a lo largo de la sección «Uso en mujeres embarazadas/lactantes» del PSUR #3, se hace la siguiente afirmación despectiva y recurrente: «»La información sobre los antecedentes obstétricos de la madre era limitada, lo que impedía una evaluación significativa»»
Mi reciente informe de investigación sobre la Revisión del Embarazo y la Lactancia de Pfizer, que acaba de publicarse en abril por orden judicial de la FDA, 2 años después de su aprobación, contenía efectos adversos condenatorios similares, como abortos espontáneos y partos prematuros de fetos expuestos a la vacuna por vía transplacentaria o transmamaria (a través de la leche materna) después de que sus madres fueran vacunadas. También se notificaron efectos adversos como parálisis facial y linfadenopatía en lactantes, expuestos indirectamente a través de la leche materna de sus madres vacunadas.
A principios de este año, Thorp et al. publicaron un artículo en el Journal of American Physicians and Surgeons que revelaba un volumen asombroso de recuentos globales de acontecimientos adversos para las vacunas COVID-19 notificados durante 18 meses, en comparación con 282 meses para las vacunas antigripales (véase la captura de pantalla de la Tabla 1 más abajo).

Dada la abundancia de pruebas condenatorias, se ha vuelto cada vez más evidente que los graves resultados negativos en el embarazo observados después de la vacunación pueden ser vistos como un factor que contribuye a la disminución de la tasa de natalidad/fertilidad, reportada en los países, que desplegaron las vacunas de ARNm.
En noviembre de 2022, se revelaron resultados impactantes en un documento de trabajo del Instituto Federal de Investigación Demográfica, titulado «Descensos de la fertilidad cerca del final de la pandemia de COVID-19»: Evidencia de descenso de natalidad en 2022 en Alemania y Suecia«.
El documento afirmaba: «La TFR mensual desestacionalizada de Alemania descendió de 1,5-1,6 en 2021 a 1,3-1,4 en 2022, un descenso de aproximadamente el 14 %. En Suecia, la TGF correspondiente bajó de aproximadamente 1,7 en 2021 a 1,5-1,6 en 2022, un descenso de casi el 10%. No existe ninguna relación entre las tendencias de la fecundidad y los cambios en el desempleo, las tasas de infección o las muertes por COVID-19. Sin embargo, existe una fuerte relación entre la tasa de fecundidad y la tasa de mortalidad. Sin embargo, existe una fuerte asociación entre el inicio de los programas de vacunación y el descenso de la fertilidad nueve meses después de dicho inicio.»
Lo que llama la atención es que incluso en la versión 9.0 del Plan de Gestión de Riesgos de la EMA, revisado en noviembre de 2022 para COMIRNATY (tanto en su versión monovalente como bivalente), en la página 111 dice: «El perfil de seguridad de la vacuna no se conoce completamente en mujeres embarazadas o en periodo de lactancia debido a su exclusión inicial del estudio clínico pivotal, sin embargo, se dispone de experiencia post-comercialización en mujeres embarazadas».
Por lo tanto, tenemos constancia de que la posición actual de la EMA es que el perfil de seguridad de la vacuna no se conoce completamente en mujeres embarazadas y lactantes.
En segundo lugar, sabemos que la EMA era plenamente consciente de las alarmantes señales de seguridad encontradas en estos Informes Periódicos de Actualización de Seguridad (incluyendo casos de ensayos clínicos y post-comercialización), documentados por primera vez en el PSUR #1 porque Pfizer y BioNTech recopilaron estos documentos de farmacovigilancia para el regulador. Sin embargo, la agencia, sorprendentemente, aprobó estos productos experimentales de ARNm como «seguros y eficaces» para mujeres embarazadas y lactantes y sigue promoviendo su uso para este grupo.
Todo esto culmina en una preponderancia de pruebas que demuestran que la agencia no sólo es culpable de no proteger a esta generación de ciudadanos europeos, sino también a la siguiente.
Sugerir una corrección