Les dernières données accablantes de l’EMA confirment son échec : Rapport PSUR No.3, effets indésirables sur la grossesse et l’allaitement
Grâce à une demande en vertu de la loi sur la liberté de l’information (Freedom of Information Act), le rapport périodique de pharmacovigilance No. 3 (PSUR n° 3) de l’UE, qui couvre la période de six mois allant du 19 décembre 2021 au 18 juin 2022, est récemment devenu disponible sur le blog autrichien de politique et sciences, tkp.
Mon analyse du PSUR No.1 a été publiée dans Children’s Health Defense Europe et couvrait les effets indésirables signalés au cours des 6 premiers mois de 2021 pour le vaccin ARNm de Pfizer-BioNTech contre la COVID-19. À l’heure actuelle, le PSUR No.2 et les annexes des PSUR No.1 et 3 n’ont pas encore été publiés.
Cet article est la première partie de l’analyse du PSUR No.3, le troisième document de pharmacovigilance sollicité par l’organisme chargé de la réglementation des médicaments dans l’Union européenne, l’Agence Européenne des Médicaments (EMA), préparé par Pfizer/BioNTech et signé par la vice-présidente pour la sécurité des médicaments chez Pfizer, Barbara De Bernardi MD, le 18 août 2022.
Aperçu des données
- 508 351 rapports de cas (individus) contenant 1 597 673 événements
- Trois fois plus de cas ont été signalés chez les femmes que chez les hommes
- 1/3 des cas ont été classés comme graves
- 3280 décès ont été signalés
- Pour 60 % des cas signalés, l’issue est inconnue ou non résolue
- 92 % des cas ne présentaient aucune comorbidité
- Le plus grand nombre de cas a été enregistré dans la tranche d’âge 31-50 ans
- L’Allemagne a enregistré le plus grand nombre de cas (22,5 % de tous les cas signalés dans le monde)
Ce rapport se concentre sur les cas d’effets indésirables liés à la grossesse et à l’allaitement dans ce rapport explosif de 396 pages.
Cas des nourrissons allaités
Il est important de noter qu’un examen plus approfondi du PSUR No. 1 a fait apparaître un élément extrêmement troublant : des effets indésirables ont été signalés chez des bébés nourris au sein, indirectement exposés au vaccin à l’ARNm de Pfizer-BioNTech par leurs mères vaccinées. La capture d’écran ci-dessous est tirée de la page 165 du PSUR No.1.

Le fait que deux cas tirés des données post-commercialisation (PM) concernent des bébés qui ont été indirectement exposés au vaccin de Pfizer-BioNTech (BNT162b2) par voie transmammaire (à travers le lait maternel) et qui ont par conséquent subi un accident vasculaire cérébral (hémorragies du système nerveux central et accidents vasculaires cérébraux) est choquant.
Ensuite, à la page 149 (capture d’écran ci-dessous), trois autres cas de bébés souffrant d’effets indésirables neurologiques, par exemple des convulsions, après avoir été indirectement exposés au vaccin via le lait maternel de leur mère vaccinée, ont été enregistrés.

Cette tendance a également été observée dans le PSUR No.3 (la capture d’écran ci-dessous est tirée de la page 80).

D’après l’analyse des doses de rappel (soit en plus des 2 doses de la série primaire), un nombre impressionnant de 455 cas ont été signalés dans les 6 mois de l’intervalle de référence (1 issu des données de l’essai clinique et 454 des données post-commercialisation) concernant des bébés dont les cas « ont été exclus en raison d’une exposition indirecte (transplacentaire/transmammaire) au BNT162b2 »
Un autre exemple, illustré par la capture d’écran ci-dessous tirée de la page 239, signale 4 cas (de bébés) ayant souffert d’effets indésirables respiratoires d’intérêt particulier (EIIP), qui ont été « jugés non contributifs et n’ont pas été inclus dans la discussion car ces cas impliquaient des expositions au vaccin pendant la grossesse de la mère ou par l’allaitement »

Dans les deux rapports PSUR, Pfizer/BioNTech donne la même raison pour expliquer pourquoi ces cas « ne sont pas inclus dans la discussion »: « jugés non-contributifs » puisqu’ils concernaient des bébés « qui ont été indirectement exposés au BNT162b2 »
Compte tenu de la gravité de cet important signal de nocivité concernant les bébés allaités, ne pas tenir compte des effets indésirables sur ces nourrissons sous prétexte qu’ils avaient été indirectement exposés au vaccin par le biais du lait maternel est répréhensible.
Selon les résultats d’une étude déterminante menée en septembre 2022 par Hanna et al. et publiée dans la revue médicale JAMA Paediatrics, les chercheurs ont trouvé des traces d’ARNm du vaccin COVID-19 dans le lait maternel des femmes allaitantes, dès l’heure qui suit la vaccination. Ils ajoutent : « Nous supposons qu’après l’administration du vaccin, les nanoparticules lipidiques contenant l’ARNm du vaccin sont transportées vers les glandes mammaires par voie hématogène et/ou lymphatique. »
Souvenez-vous de l’affirmation inébranlable, mais totalement infondée, proclamée par les agences de réglementation des médicaments et les autorités sanitaires du monde entier, selon laquelle le vaccin ARNm reste dans le bras? Eh bien, rien n’est plus faux!
Dans une lettre récente, obtenue clandestinement, de la directrice exécutive de l’EMA, Emer Cooke, à la présidente du comité spécial COVID-19, l’eurodéputée Kathleen Van Brempt, Cooke admet à contrecœur « que les nanoparticules lipidiques peuvent se répartir de manière non spécifique dans plusieurs organes tels que le foie, la rate, le cœur, les reins, les poumons et le cerveau, le foie semblant être l’organe où les nanoparticules lipidiques se répartissent le plus »
Son aveu suit de près le rapport d’évaluation de l’agence du médicament australienne, la Therapeutics Goods Administration (TGA), sur l’étude de biodistribution non clinique de Pfizer, mise en évidence par le député européen Robert Roos lors de l’audition du 27 mars 2023 de la commission spéciale sur le COVID-19. Le rapport de la TGA de janvier 2021 a révélé de manière alarmante que les nanoparticules lipidiques qui renferment l’ARNm atteignent le foie, la rate, le cerveau, les yeux, la moelle osseuse, les glandes surrénales, les ovaires et les testicules, c’est-à-dire presque tous les tissus organiques.
Les cas des grossesses (données cumulées des essais cliniques)
Les cas portant sur les grossesses qui ressortent des données cumulées des essais cliniques dans le PSUR N° 3 proviennent des essais cliniques des phases 1/2/3 menés par Pfizer jusqu’en juin 2022. Bien que les femmes enceintes aient été exclues de l’essai pivot de Pfizer, certaines des participantes sont tombées enceintes. Dans le cadre de la lettre d’approbation pour l’utilisation d’urgence de COMIRNATY (nom commercial du vaccin ARNm de Pfizer-BioNTech), l’Organisation mondiale de la santé (OMS) a demandé à BioNTech, titulaire de l’autorisation de mise sur le marché, de surveiller ce qui était advenu de ces femmes enceintes.
697 cas cumulés de grossesse ont été signalés, dont 597 cas concernant la mère et 100 cas concernant le bébé/fœtus. Dans 431 cas, l’exposition au vaccin in utero a été signalée sans qu’aucun événement clinique ne se soit produit chez la mère. Voici une ventilation des 166 cas de mères qui ont signalé des événements cliniques indésirables. Les chiffres entre parenthèses indiquent le nombre d’événements signalés.
- ~ Environ 1/5 de tous les cas mères ont signalé des événements indésirables graves (139)
- avortements spontanés (46)
- Pré-éclampsie (7)
- Disproportion céphalo-pelvienne (6)
- Avortement manqué, mort fœtale, hémorragie post-partum, séparation prématurée du placenta (4 chacun)
- Menace d’avortement, grossesse extra-utérine, hypertension gestationnelle, accouchement prématuré, accouchement prématuré (3 chacun)
- Avortement incomplet, hyperémèse gravidique, exposition de la mère par son partenaire pendant la grossesse, fausse couche du partenaire, troubles utérins (2 chacun)
- COVID-19 (9)
- Anémie (2)
Dans la liste ci-dessus, il convient de souligner que « l’exposition de la mère par son partenaire pendant la grossesse » et « la fausse couche du partenaire » se réfèrent à des cas de femmes indirectement exposées au BNT162b2 par leurs partenaires vaccinés. Ce point important concerne l’excrétion vaccinale, qui était dans le collimateur de Pfizer avant même le début de l’essai clinique, mais qui a ensuite été largement présentée comme un mythe au public. Selon le protocole d’essai clinique de Pfizer, les cas de femmes enceintes indirectement exposées au vaccin par leurs partenaires (qui ont participé à l’essai) faisaient l’objet d’une classification particulière (« expositions pendant la grossesse ») et devaient être immédiatement signalés à Pfizer en tant que “événement indésirable grave du vaccin” et ce, dans les 24 heures, par l’investigateur clinique. La grossesse devait être suivie par cet investigateur et Pfizer Safety devait être informé de l’issue de la grossesse.
Les cas des bébés/fœtus (données cumulatives des essais cliniques)
Ce qui est troublant, c’est que 98 des 100 cas signalés portant sur des bébés/fœtus sont considérés comme graves. Les captures d’écran ci-dessous évoquent des effets effroyables.

Pour les 68 cas de bébés/fœtus dans la catégorie « naissance vivante sans anomalie congénitale », des effets indésirables graves ont cependant été signalés et sont listés dans la capture d’écran ci-dessous.

Il y a également eu un cas de mortinaissance sans anomalie fœtale au cours de la période de référence, qui a été codé comme syndrome de détresse respiratoire néonatale.
Les cas des grossesses (d’après les données post-autorisation)
Selon les données post-autorisation, il y a eu 3642 cas impliquant des grossesses et 1898 issues de grossesse au cours de la période de référence (décembre 2021-juin 2022). L’Allemagne a enregistré le plus grand nombre de cas d’effets indésirables sur les grossesses (837) au cours de la période de référence, suivie par le Royaume-Uni avec 475 cas. Le tableau de ces 1898 résultats est présenté ci-dessous.
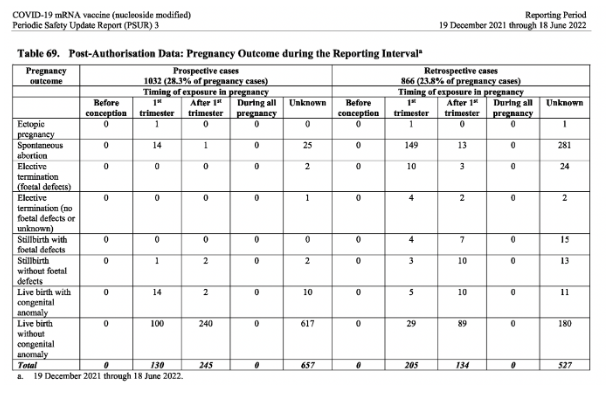
Il est important de noter qu’un tiers des issues de grossesse fournis au cours de la période considérée étaient négatives.
Avortement spontané : 483
Naissance vivante avec anomalies congénitales : 52
Mortinaissance avec malformations fœtales : 26
Interruption volontaire de grossesse (en raison de malformations fœtales) : 39
Sur les 3642 cas de grossesse, 322 ont été classés comme des cas de bébés/fœtus et 3320 comme des cas de mères.
Les cas bébés/fœtus (données post-autorisation)
90 % des 322 cas de bébés/fœtus ont été classés comme graves. Il y a eu 39 cas de « naissance vivante avec anomalie congénitale » Les captures d’écran ci-dessous montrent l’éventail effrayant de ces anomalies.

Parmi les cas de nouveaux-nés, 37 cas d’avortement spontané ont été signalés avec les événements suivants : « retard de croissance fœtale (18), anomalie congénitale (8), rythme cardiaque fœtal anormal (3), anomalie cytogénétique, malperfusion vasculaire fœtale (2 dans chaque cas) »
Dans 4 cas, la mère avait des antécédents médicaux sous-jacents, mais pour les 33 autres cas, le rapport indique que « les informations concernant les antécédents obstétriques ou les médicaments pris par la mère étaient limitées, ce qui a empêché une évaluation significative du lien de causalité »
Vingt-trois cas d’interruption volontaire de grossesse ont été signalés. 22 de ces 23 cas « ont fait l’objet d’une interruption volontaire de grossesse en raison de malformations fœtales » Il y a eu 21 autres cas de mortinaissances, dont un peu plus de 70 % étaient dus à des malformations fœtales.
En contraste frappant avec ces données accablantes, le rapport conclut :aucun signal de risque concernant l’utilisation chez les femmes enceintes ou allaitantes n’est ressorti de l’examen de ces cas«
En outre, tout au long de la section « Utilisation chez les femmes enceintes/allaitantes » du PSUR n°3, on trouvait la déclaration désinvolte et récurrente suivante : « Les informations concernant les antécédents obstétriques de la mère étaient limitées, ce qui a empêché une évaluation significative »
Mon récent rapport d’enquête sur le compte rendu de Pfizer concernant la grossesse et l’allaitement, lequel vient d’être publié en avril par la FDA suite à une injonction, deux ans après sa signature, fait état d’effets indésirables similaires, tels que des avortements spontanés et des accouchements prématurés de fœtus exposés au vaccin par voie transplacentaire ou transmammaire, suite à la vaccination de la mère. Des effets indésirables tels que la paralysie faciale et la lymphadénopathie ont également été signalés chez des nourrissons indirectement exposés par le biais du lait maternel de leur mère vaccinée.
Au début de cette année, un article a été publié dans le Journal of American Physicians and Surgeons par Thorp et al. qui a révélé un volume étonnant d’effets indésirables pour les vaccins COVID-19 dans le monde, signalés sur 18 mois, contre 282 mois pour les vaccins antigrippaux (voir la capture d’écran du tableau 1 ci-dessous).

Compte tenu de l’abondance de preuves accablantes, il est de plus en plus évident que les issues négatives de grossesse observées après la vaccination doivent être considérées comme un facteur contribuant à la baisse du taux de natalité/fertilité, signalée dans les pays qui ont déployé les vaccins à ARNm.
En novembre 2022, des résultats choquants ont été révélés dans un document de travail de l’Institut fédéral de recherche sur la population, intitulé « Déclin de la fertilité à la fin de la pandémie COVID-19 : Signes d’une baisse de la natalité en 2022, en Allemagne et en Suède ».
Le document indique que « l’ISF (Indice Synthétique de Fécondité) mensuel et corrigé des variations saisonnières est passé en Allemagne de 1,5-1,6 en 2021 à 1,3-1,4 en 2022, soit une baisse d’environ 14 %. En Suède, l’ISF correspondant est passé d’environ 1,7 en 2021 à 1,5-1,6 en 2022, soit une baisse de près de 10 %. Il n’y a pas d’association entre l’évolution de la fécondité et des changements dans les taux de chômage, d’infection ou de décès COVID-19. Cependant, il existe une forte association entre le début des programmes de vaccination et la baisse de la fécondité neuf mois après ce début« .
Ce qui est remarquable, c’est que même dans la version 9.0 du plan de gestion des risques de l’EMA, révisée en novembre 2022 pour COMIRNATY (versions monovalente et bivalente), on peut lire à la page 111 : « Le profil de sécurité du vaccin n’est pas entièrement connu chez les femmes enceintes ou allaitantes en raison de leur exclusion initiale de l’étude clinique, mais l’expérience post-commercialisation chez les femmes enceintes est disponible ».
Nous savons donc que pour l’EMA actuellement, le profil de sécurité du vaccin n’est pas entièrement connu chez les femmes enceintes ou allaitantes.
Deuxièmement, nous savons que l’EMA était parfaitement au courant des risques alarmants émergeant de ces rapports périodiques de pharmacovigilance (comprenant les essais cliniques et les cas de post-commercialisation), documentés pour la première fois dans le PSUR No.1, parce que Pfizer et BioNTech ont compilé ces documents de pharmacovigilance justement pour l’EMA. Pourtant, l’agence a scandaleusement approuvé ces produits expérimentaux à base d’ARNm comme étant « sûrs et efficaces » pour les femmes enceintes et allaitantes et continue à ce jour à promouvoir leur utilisation pour cette cohorte.
Tout cela aboutit à une prépondérance de preuves montrant que l’agence est non seulement coupable de ne pas avoir protégé la génération actuelle de citoyens européens, mais aussi la suivante.
Suggérer une correction







