Писма от подземния свят
ИЗОБРАЖЕНИЕ ОТ: Shutter Stock
Преразглеждане на изтеклите от ЕМА (Европейската Агенция по Лекарствата) имейли
В края на 2020 г. колекция от документи – приблизително 900 страници от раздела за „ваксината“ на Pfizer „Химично производство и контрол“ (MCM) от регулаторното заявление до Европейската агенция по лекарствата (EMA), изтекоха и бяха изпратени на редица журналисти. Документите включваха и размяна на имейли между някои от проверяващите и висши ръководители в ЕМА. Изтичането беше отразено в British Medical Journal, който успя да потвърди, че документите са автентични. Получих тези документи от колега около година по-късно, в края на 2021 г., и прочетох и използвах голяма част от тях в анализите си. В професионалната си работа съм виждал много документи, свързани с научноизследователската и развойната дейност на Пфайзер, така че също мога да потвърдя, че тези, които изтекоха, бяха в голяма степен съвместими с типичната документация на Пфайзер. ЕМА не отрече автентичността, а само заяви, че заглавията на някои от имейлите са били променени.
Сега имам много по-голям брой последователи и много по-ясна представа за организацията и псевдоправната структура на престъпния картел, който движи глобалното зверство, разговорно известно като „отговор на ковид пандемията“. Връщам се отново към изтеклите имейли, тъй като смятам, че те предоставят някои изключително важни доказателства.
Файловете с имейли на ЕМА, които прочетох, съдържат 14 скрийншота на имейли от средата до края на ноември 2020 г. Разменените писма са от служители на ЕМА и висши ръководни кадри. По мое мнение тези имейли показват, че:
- Рецензентите на ЕМА са били подложени на огромен политически натиск да измислят нови начини за одобряване на неодобрените опасни продукти. Натискът е идвал от самите върхове на правителствата на САЩ, Обединеното кралство и ЕС.
- Комисарят на ЕС Урсула фон дер Лайен е дала обещания на държавите-членки, които никога не е възнамерявала да изпълни, за да ги обвърже с единен пакт за договорите за ваксини и по този начин да изпревари всякакви независими решения в собствените им страни.
- Съществуваха сериозни и неразрешими – предвид умишлено нереалистичните срокове – проблеми с качеството на продукта, които служителите на ЕМА бяха принудени да одобрят. Някои от тях се чувстваха неудобно да го направят и да изразят опасенията си. Други „пренебрегваха“ очевадно измислени данни.
В крайна сметка самият регулаторен преглед и изразените опасения нямаха значение – продуктът щеше да бъде пуснат на пазара независимо от това. Сега вече знаем точно защо – регулаторните органи не са имали необходимата регулаторна власт над него. Фармацевтичните регулаторни органи не контролират военните материали, известни като „контрамерки“ и „производствени демонстрации“ (ефимизми, прикриващи биологичните бойни вещества, произведени от плененото правителство на САЩ и неговите глобални партньори). Електронните писма показват, че по-голямата част от служителите на ЕМА са били неволни участници в тази пиеса.
Наскоро излезе потвърждение на това за Обединеното кралство.
Въз основа на отговора на MHRA FOIA (Агенция за регулиране на лекарствата и здравните продукти, Закон за свобода на информацията, бел. пр.)
„Всички решения за издаване на разрешения за ваксини и терапевтични продукти на Covid са взети от министъра на лицензирането и не са били делегирани“
Превод – обикновено правомощията за преглед и одобрение на нови фармацевтични продукти са официално делегирани на MHRA от държавния министър на здравеопазването (Обединеното кралство). В случая с ковид продуктите делегирането на правомощия не съществува. Оказва се, че всички те са разгърнати еднолично от Мат Ханкок (въпреки че той сочи с пръст някой по-висшестоящ). Същото се случи и в САЩ – Алекс Азар при администрацията на Тръмп разгърна тези несъответстващи на изискванията биоматериали върху американците, а Хавиер Бекера при Байдън продължава да го прави и днес.
Политическият натиск.
На 16 ноември 2020 г. между висши ръководни кадри на ЕМА се състоя следната размяна на имейли:
Ноел Уатийон – заместник-изпълнителен директор (пенсиониран през юни 2021 г.):

Агнес Сен-Реймон – ръководител на отдел „Международни отношения“:

Марко Кавалери – председател на работната група по пандемията Covid-19 в ЕМА:

Имейлите трябва да се четат отдолу нагоре.

Няколко интересни неща: и трите регулаторни органа – FDA на САЩ, MHRA на Обединеното кралство и EMA на ЕС – са заети с координиране на сроковете за одобрение, преди да е извършен какъвто и да е официален преглед на данните, преди консултативните комитети да са видели резултатите от клиничните изпитвания, да са ги обсъдили, да са гласували по тях и т.н. Те обсъждат сроковете, тъй като данните НЯМАТ значение за това дали тези продукти ще бъдат пуснати на пазара или не. Освен това те си взаимодействат така, сякаш не са три отделни агенции на отделни суверенни държави, отговорни пред отделни групи данъкоплатци и конгресен/парламентарен надзор, а просто бюрократични отдели, вече слети в едно глобално правителство. И накрая, FDA ще се „втурне за EUA (Разрешение за използване при спешни случаи)“, като е „тласкана от Азар“ (Алекс Азар – министър на здравеопазването по онова време) и „Тръмп дърпа конците“.
Много хора ме питат как е възможно хиляди хора да са участвали в измамата, организирана като „отговор на ковид пандемията“ – със сигурност не е възможно толкова много хора да са в сговор! Не е било необходимо толкова много хора да са в течение. Тук Ноел Уатийон, висш ръководител на ЕМА, или не знае, че прегледът на данните е без значение за това дали инжекциите в крайна сметка ще бъдат пуснати на пазара, или умело изопачава това (всъщност вярвам, че не е знаел). Следователно служителите на ЕМА под него не би трябвало да са наясно и просто да бързат да свършат каквато и да е специфична задача, която им е възложена. Разделянето на службите е ключът към прикриването на всяка голяма измама в големите организации и сложните структури. Затова ли е подал оставка/пенсионирал се е малко след разгръщането на смъртоносните инжекции? Той също така е подложен на натиск от страна на ЕК (Европейската комисия) да ги одобри. А Пфайзер сега иска пълно разрешение за употреба вместо условно такова! Забележете – условното разрешение за употреба е издадено, но условията така и не са изпълнени от Pfizer/BioNTech, защото на кого му пука, това си беше игра от самото начало.
„(Co)-Rapps“ = съдокладчици. ЕМА е европейска структура, съставена от бившите отделни „компетентни органи“ на държавите членки, които регулираха и одобряваха фармацевтичните продукти във всяка страна поотделно. В европейската структура екипът за технически преглед и съпреглед се избира за конкретен продукт. В случая с ковид „ваксините“ шведският екип, ръководен от Филип Йозефсон, беше докладчик (водещ рецензент), а френският екип, ръководен от Жан-Мишел Рейс – съдокладчик. „CHMP“ =Комитет за лекарствени продукти за хуманна употреба (КЛПХУ) (към ЕМА).

Електронното писмо е адресирано до Олга Соломон в ЕК (Европейската комисия), а копие е изпратено до шефа на Ноел, Емер Кук -изпълнителен директор на ЕМА и бивш висш ръководител в СЗО. Това е Емер Кук:

Умният пакт на Урсула.
Помните ли я?

Урсула фон дер Лайен – комисар на ЕС, чиито постижения включват договаряне на невероятни хищнически договори за доставка на Pfizer от името на всички държави-членки на ЕС чрез текстови съобщения с главния изпълнителен директор на Pfizer Алберт Бурла. В тези договори страните от ЕС трябваше да предоставят държавни активи като обезпечение, да се откажат от всички закони за контрол на качеството, вноса и защитата на потребителите и да се откажат от националния суверенитет – т.е. да не могат да променят законодателството по отношение на отговорността за ваксините от собствените си парламенти? Хищническите договори, които бяха напълно редактирани, за да се защитят така наречените „търговски интереси на Pfizer“. Следната размяна на имейли е свързана с доблестните усилия на Урсула:

Използвани са куп съкращения, като най-съществените са: „ЕК“ = Европейска комисия, „ДЧ“ = държави членки, „ЕП“=Европейски парламент. Ключовото изречение е, че Урсула е „готова да се обади лично на съответните министри на здравеопазването, за да се избегне използването на член 5, параграф 2“. За какво става дума? Чл. 5, ал. 2 се отнася до „чл. 5, ал. 2 от Директива 2001/83“ – разрешение за спешна употреба в европейска държава членка, което се дава от всяка от държавите членки поотделно в собствените им държави. CMA е условно разрешение за пускане на пазара, което се издава от EMA за всички членове на ЕС едновременно. Рекламирано от ЕС като много по-стабилен процес от този за Разрешение за използване при спешни случаи на ЕС (подчертаването е добавено от мен):
…CMA следва контролирана и стабилна рамка, осигуряваща гаранции, каквито разрешенията за спешна употреба не могат да предоставят. В действителност разрешението за спешна употреба не е разрешение за ваксината, а разрешение за временна употреба на неразрешена ваксина. CMA гарантира, че всички изисквания за фармакологична бдителност, производствен контрол, включително контрол на партидите за ваксини, и други задължения след издаване на разрешението се прилагат по правно обвързващ начин […]. В частност:
– Осигурява строг мониторинг, чрез системата на ЕС за фармакологична бдителност, за безопасността на лекарството в целия ЕС. […]
-Осигурява наблюдение на безопасността след издаване на разрешението и позволява събирането на допълнителни данни по структуриран начин. […].
–Строго контролирано производство, включително освобождаването на партиди за ваксини и дистрибуцията, са обект на същия текущ контрол, както за всички разрешени за употреба лекарства. Наблюдението на производствените процеси гарантира, че лекарството се произвежда и контролира в съответствие с високите фармацевтични стандарти в контекста на широкомащабната комерсиализация.
При условно разрешение за пускане на пазара на ЕС (CMA) отговорността е на притежателя на разрешението за пускане на пазара. Притежателят на разрешението за търговия ще носи отговорност за продукта и неговата безопасна употреба.
На теория това звучи страхотно. Това обеща Урсула, когато лично се обаждаше и извиваше ръцете на политиците на държавите членки. Може би извиването на ръцете дори не е било необходимо, тъй като те са били достатъчно тероризирани от ковидната пропаганда и са очаквали чудодейните „ваксини“ да ги спасят. Проблемът е, че Урсула никога не е възнамерявала да изпълни тези обещания, а и във всеки случай не е възможно да се произвеждат мРНК „ваксини“ с безопасността, ефикасността и качеството на производство, които се изискват за фармацевтичните продукти. Това, от което Урсула наистина се нуждаеше в този процес, беше да обвърже всички европейски държави-членки в пакт, като обещае „железна“ процедура за условно пускане на пазара (CMA), така че те да не могат да имат независим орган върху инжекциите, разпространявани в техните страни. Пътят по член 5 щеше да означава, че всяка държава членка може да разрешава продукта, а след това щеше да има право да отменя разрешението, ако открие някакви проблеми. Член 5 предвижда също така освобождаване на производителя от отговорност, което обаче прави невъзможно издаването на разрешение за продукта. С пътя на CMA нито една от държавите-членки не би могла да упражни правото си на независимо вземане на решения и така тя би могла да ги принуди да сключат едни и същи, безумни и почти напълно редактирани договори с Pfizer, Moderna и AstraZeneca, които така или иначе освобождават от всякаква отговорност и освен това забраняват на държавите да променят собствените си закони по отношение на отговорността!
Купувачите трябва да „обезщетят, защитят и предпазят Pfizer … от и срещу всички съдебни искове, претенции, действия, искания, загуби, щети, отговорности, споразумения, санкции, глоби, разходи и разноски … произтичащи от, свързани с или произтичащи от ваксината“
Забележими основни възражения и липсата на такива от страна на проверяващите от ЕМА.
Разделът „Химично производство и контрол“ (CMC) на Заявлението за лиценз за биологично лекарство е основният стълб на регулаторното одобрение. В него се описва производственият процес и съответствието с добрите производствени практики (cGMP), както и обширен набор от закони и разпоредби, предназначени да осигурят чистотата, ефикасността, последователността и безопасността на масово произвежданите лекарства и биологични продукти. Данните за безопасност и ефикасност от клиничните изпитвания са безполезни, ако производителят не може да увери регулаторните органи и медицинската общност, че:
- съответният продукт по спецификация е използван в клиничните изпитания;
- продуктът е последователно произведен, чист, висококачествен, възпроизводим, с добре охарактеризиран и предвидим производствен процес и етапи на контрол;
- същият продукт, който е бил изпитван, ще бъде разпространяван в търговската мрежа;
Бяха установени проблеми в раздела за CMC на подаденото от Pfizer заявление:

Оценителите от CMC не бяха доволни от срока, даден за оценка, тъй като той нарушаваше всички нормални срокове и всички ускорени срокове, при това с голяма разлика. Затова решението беше, че оценителите просто трябва да бъдат „натиснати“. Така се постигна само една цел – да се принудят хората, които потенциално биха могли да изкажат опасения, да бъдат доведени до ръба на изтощението, така че те просто да се откажат и да се съгласят. В края на краищата тези на върха добре знаеха, че регулаторният преглед няма никакво значение и никакво отражение върху фалшивото „одобрение“, той щеше да се случи независимо от всичко. В Обединеното кралство MHRA вече призна, че не е имала официално делегирани правомощия да преглежда и одобрява тези инжекции, и съм готов да се обзаложа, че и EMA не е имала такива правомощия.
Оценителите на ниско ниво в CMC не са знаели това и са работили много усърдно и най-вероятно добросъвестно. До края на ноември те повдигнаха над 140 официални възражения срещу подадената от Pfizer за CMC заявление, в която все още имаше много пропуски и липсваща информация. За справка: 10-15 регулаторни възражения обикновено спират движението на фармацевтичното заявление, докато възраженията не бъдат отстранени. Три основни възражения, т.е. официални червени флагове, са разгледани конкретно в имейлите по-долу. Аз и други писахме подробно за МО№2 (липса на интегритет на мРНК). Ето имейл от един от проверяващите, Евдокия Коракианити, и отговор от Алексис Нолте, в който се обсъжда проблемът и въздействието (напълно неизвестно и потенциално много обезпокоително) върху ефикасността и безопасността на продукта:

Проблемът с разграждането на мРНК беше обсъден и от специалистите по качеството на CMC Тон ван дер Стапен, старши експерт по биофармация в Съвета за оценка на лекарствата (базиран в Нидерландия) и специалист по качеството на ЕМА:

и Брайън Дули, друг фармацевтичен специалист по качеството в ЕМА:

Снимките по-долу са от прегледа на качеството, представен от тях на ЕМА. Първата снимка е посветена на вече добре документирания проблем с разграждането на мРНК в различни партиди от продукта на Pfizer. Тук резултатите от анализа на партидите, предоставени от Pfizer, са изброени и цветно кодирани по различни места на производство, както и по лекарствени вещества и категории лекарствени продукти. Лекарствено вещество = активните компоненти на продукта (само мРНК), а лекарственият продукт е веществото, формулирано в липидите и другите съставки. Цялостта на % мРНК описва % на откритата в партидата мРНК с „пълна дължина“. Другата част от партидата е съставена от неизвестни накъсани парчета с неизвестни свойства или въздействие върху безопасността. Обърнете внимание, че регулаторните органи не са извършили никаква независима проверка, а просто са посочили цифрите, предоставени от Pfizer/BioNTech.
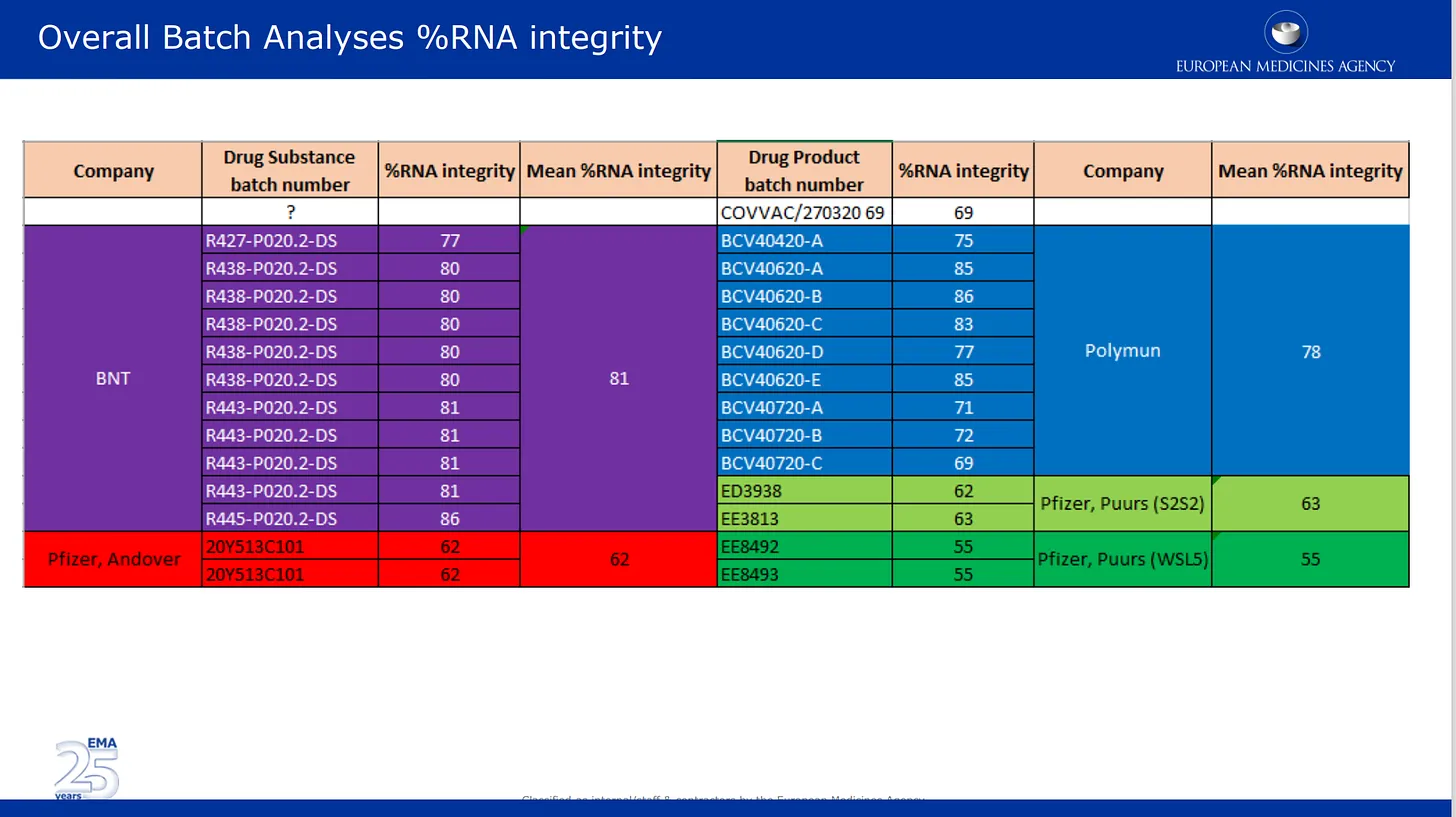
Оказва се, че тези двама научни консултанти са прегледали и приели фалшивите изображения на резултатите от Western blot(широко използвана аналитична техника в молекулярната биология, имуногенетиката и други молекулярни биологични дисциплини за откриване на специфични протеини в проба от тъканен хомогенат или екстракт. бел. пр.), представени от Pfizer на EMA – ето ги в собствената им PowerPoint презентация за преглед от 24 ноември 2020 г. Прочетете бележката под слайда – те приемат тези изображения като истински, въпреки че и двамата рецензенти би трябвало да знаят по-добре. Защо НЕ са се противопоставили на това? Ето какво се казва в бележката:
Размерът на белтъка след ин-витро експресия на лекарственото вещество BNT162b2 беше определен с помощта на Western blot. Беше потвърдено, че размерът на експресирания протеин е съпоставим за трите партиди от Процес 1 и партидата от Процес 2. Фигура 3.2.S.2.6-15 показва, че размерът на експресирания протеин съответства на очаквания размер на лекарственото вещество BNT162b2 и е сравним за всички тествани партиди. Освен това относителните нива на експресия са сравними за всички партиди, както се вижда от сравнимия интензитет на ивицата при всяко ниво на натоварване във всички партиди.

Може би някои сериозни журналисти, трябва да се обърнат към д-р ван дер Стапен и д-р Дули, както и към г-жа Коракианити и другите лица, споменати тук, за коментар.
От отговорите, повдигнати от Евдокия Коракианити, става ясно, че ръководството на ЕМА е вдигнало рамена и е разчитало на „данни, които само FDA е виждала“, но е „оптимистично“ настроенио и че FDA твърди, че разкъсването на мРНК е „теоретична загриженост“. Наистина? Има ли някакви данни в подкрепа на това твърдение или не? Ето имейлите, които показват, че основните възражения са били официално написани и впоследствие пренебрегнати от ЕМА, тъй като продуктът е бил доставен в търговската мрежа само няколко седмици по-късно. Условията на CMA никога не са били изпълнени.
Това потвърждава това, което вече знаем – нито ЕМА (нито FDA, Health Canada, MHRA или други регулаторни органи) е имала реални правомощия по отношение на тези продукти или влияние върху това дали те ще бъдат внедрени върху нищо неподозиращата общественост. Всичко това беше театър от началото до края.
Ето трите Основни Възражения (ОВ), които остават неразрешени до момента:

А ето и махането с ръка и приемането на твърденията на FDA без никакво разпитване или официална оценка на данните от страна на регулаторните органи на EMA:

Това, което мога да кажа в заключение – преброих приблизително 70 различни лица, споменати в изтеклите документи и имейли, които са улеснили този панаир на трагедията – „одобрението“ на най-смъртоносния продукт, пускан някога върху най-голям брой хора, което доведе до безпрецедентен брой смъртни случаи и наранявания по целия свят. Може би, с няколко изключения, повечето от тях са били измамени през 2020 г. и не са разбрали, че участват във военно престъпление и подписват смъртоносна измама. Вярвам, че повечето от тях вече знаят, надявам се да са достатъчно ужасени от това, което са позволили, и се надявам тези хора да излязат напред като информатори и да започнат да говорят. Имаме нужда от отговори.
Първоначално публикувано от Due Diligence and Art
Suggest a correction