Стряскащи доказателства сочат, че BioNTech/Pfizer са фалшифицирали ключови данни и допълнителни скандали (част 2)

Първоначално публикувано в Trial Site News
Част 1 от моя разследващ доклад, публикуван в Trial Site News, беше посветена на необичайно изглеждащите „Western Blots“ на Pfizer-BioNTech – скандалът, известен като Blotgate. Western Blots бяха извършени от BioNTech, за да докажат верността на своя продукт (пред регулаторните органи), че само очакваният протеинов шип е експресиран инвитро от модифицираната ваксинална мРНК и че той е последователен между различните партиди.
Проблемът с факта, че те не изглеждат като автентични/конвенционални Western blots, а по-скоро като компютърно генерирани версии (автоматизирани Western blots, въпреки че не са обозначени като такива в нито един от докладите), е отклоняване на вниманието от истинския скандал: доказателствата, които на пръв поглед показват, че BioNTech/Pfizer са „изкопирали“ тези ленти, с други думи, фалшифицирали са ключовите си данни. Тези очевидно изфабрикувани западни ленти (показани по-долу) бяха разкрити в отговора на Pfizer на въпроси от Американската агенция по храните и лекарствата около ноември 2020 г., в периода преди одобрението за спешна употреба.
Едва когато тези ленти бяха количествено определени с помощта на софтуерен анализ на изображенията (благодарение на анонимен експерт), работата на „изкопиране“, извършена върху 4 отделни партиди от техния продукт, трансферирани при 6 различни концентрации, стана поразително видима.
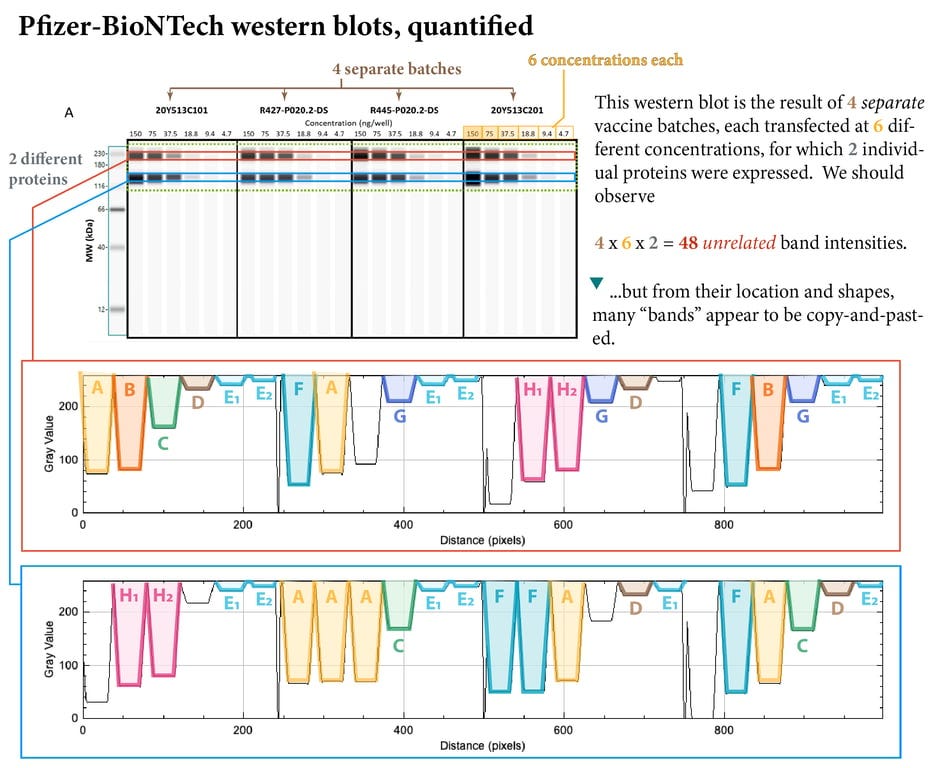
Текст изображение: „Този Western blot е резултат от 4 отделни партиди ваксини, всяка от които е трансфектирана с 6 различни концентрации, за които са експресирани 2 отделни протеина. Трябва да наблюдаваме: 4 x 6 x 2 = 48 несвързани интензитета на лентите.
…но по разположението и формата им много ленти изглеждат „изкопирани“.“
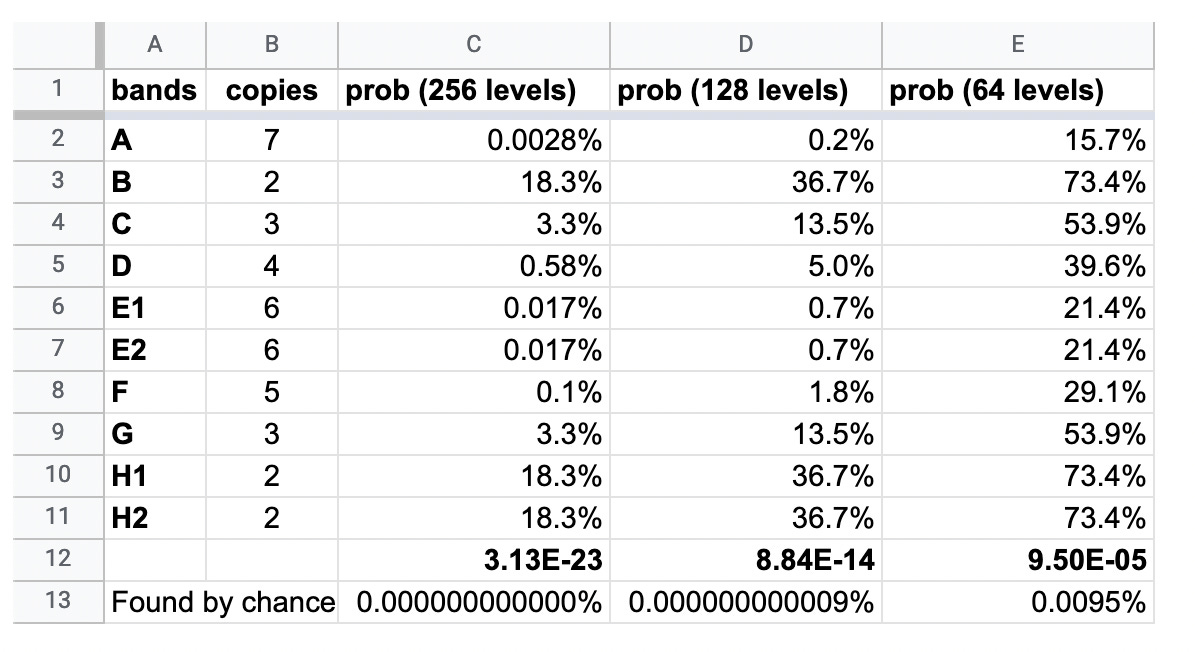
Шансовете за естествено възникване на абсолютно същите ленти в четири отделни партиди ваксина, трансфектирани при 6 различни концентрации, могат да се видят в таблицата по-долу.
По петите на част 1 от моя разследващ доклад, Epoch Times проведе собствено разследване на Blotgate; проблемите с качеството на мРНК на ваксините Pfizer-BioNTech и се позова на разследването на Trial Site News за изтичането на имейли и документи от Европейската агенция по лекарствата (ЕМА).
„Скриване на мръсните ленти“ – допълнителен поглед към Blotgate
На 13 януари, малко след избухването на скандала Blotgate, статията, спонсорирана от Pfizer и BioNTech, Patel et al. със заглавие „Characterization of BNT162b2 mRNA to Evaluate Risk of Off-Target Antigen Translation“ (Характеризиране на BNT162b2 мРНК за оценка на риска от транслация на нецелеви антиген) беше публикувана на в Journal of Pharmaceutical Sciences. В статията има много аномалии и си струва да се отбележи, че специалистът по компютърна и молекулярна биология, д-р Джесика Роуз, е написала подробен критичен анализ на това изследване.
Първо, заслужава да се отбележат конкурентните интереси на авторите, които могат да се видят по-долу.

Текст изображение:
„Декларация за конкурентен интерес. Авторите декларират следните финансови интереси/лични взаимоотношения, които могат да се разглеждат като потенциални конкурентни интереси: Химакши К. Пател, Кун Джан, Рейчъл Утегг, Илейн Стивънс, Шона Салем, Хайди Уелч, Джеф Райчек, Дейвид Джей Сирели и Томас Ф. Лерх са служители на пълен работен ден и може да са акционери на Pfizer Inc. Свеня Гробе, Юлия Шлерет и Андреас Н. Хун са служители на пълен работен ден и може да са акционери на BioNTech SE.
Финансиране: Това проучване е подкрепено от Pfizer Inc. и BioNTech SE.“
В разговор с д-р Джесика Роуз, която интензивно е извършвала конвенционални Western Blots, тя обясни: „Според моето експертно мнение [традиционният Western] е един от тестовете на стенда, който е процедура, подобно на тестването за безопасност на биологичните продукти (което трябва да отнеме 10 години). Western blot изисква последователност от специфични стъпки, тези стъпки не могат да бъдат прибързани и не могат да се припокриват… експериментите, извършени с помощта на Robo Jess [автоматична машина за Western blot] и блотовете, представени от Pfizer, трябва да могат да бъдат възпроизведени от човешка ръка, възпроизводимостта е изискване, особено когато списъкът с конфликти на интереси е толкова дълъг от страна на представящите автори [Patel et al.].“
Изображението по-долу, взето от статията на Patel et al. показва техния „Western Blot“ Забележете много дебелите (хомогенни) черни правилни ленти, без никакви размазвания.
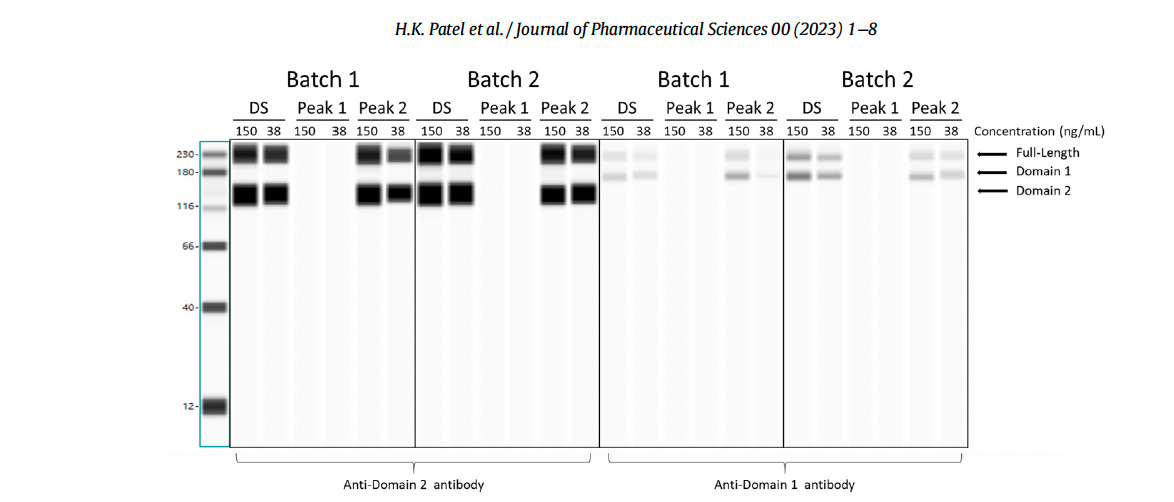
Същият „Western Blot“ (видян по-долу), само че в много по-груба, копирана версия, може да бъде намерен в редактирания доклад на CHMP (Комитет за лекарствени продукти за хуманна употреба) на Европейската агенция по лекарствата от август 2021 г., около 18 месеца преди статията на Patel et al.
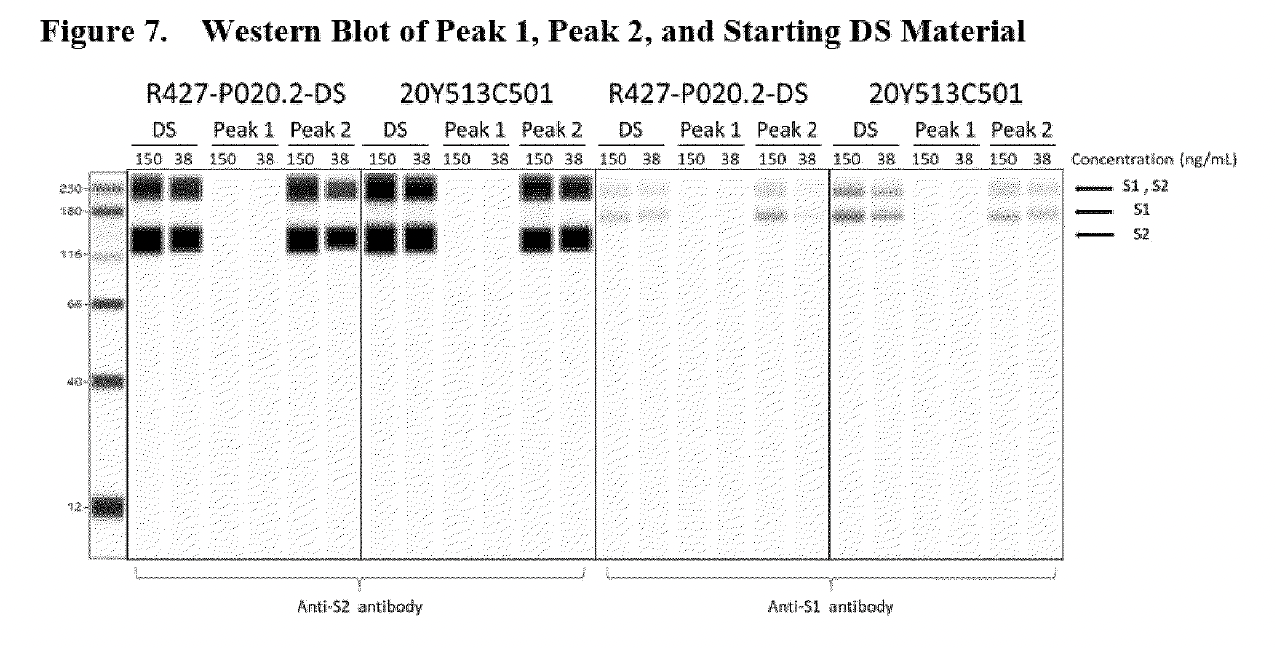
Тъй като авторите Patel et al. се позовават на технологията ProteinSimple в своето проучване (откъс по-долу), може да се направи сравнение с автоматизирана проба Western blot, използваща софтуера на същата компания.
„Клетъчните лизати бяха анализирани със специфични антитела за откриване на шипови протеини на SARS-CoV-2 с помощта на технологията ProteinSimple. Използвани са модул за разделяне на 12-230 kDa Wes и 25 капилярни касети. Бяха използвани антитела срещу миши SARS-CoV-2 Spike S1 субединица (R&D systems, каталожен № MAB105403) и антитела срещу миши SARS-CoV-2 Spike S2 субединица (R&D systems, каталожен № MAB10557). Резултатите от пробите с мРНК са докладвани като изображения на ProteinSimple Wes
Източник: Patel et al
Изображението по-долу представя автоматичен Western, използващ технологията ProteinSimple.
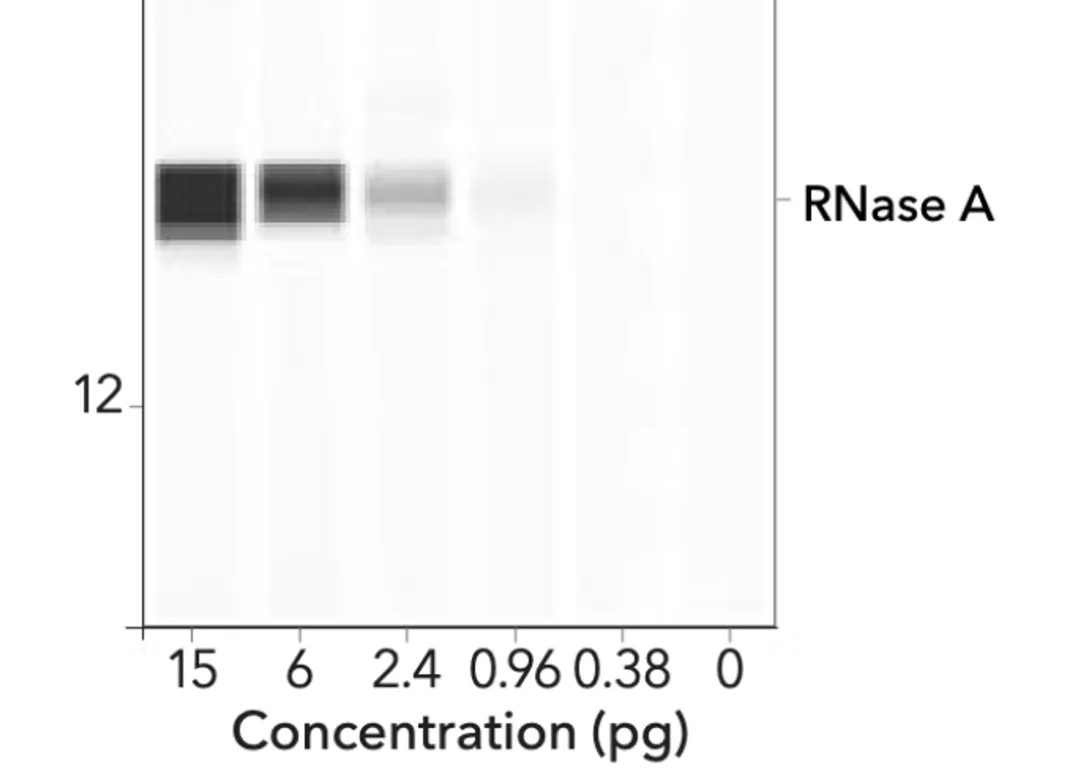
Това, което прави впечатление, е, че във всяка от разнообразните ленти може да се види градиент (ефект на размазване). Те изглеждат съвсем различно от плътните, хомогенни черни ленти на BioNTech/Pfizer.
За да получим повече информация, интервюирахме Кевин МакКернън, ръководител на научноизследователската и развойната дейност на Проекта за човешкия геном и учен в областта на геномиката, който обясни, че „ данните на BioNTech/Pfizer са неизползваеми“ и че неговото обяснение за необичайния вид на лентите на Western Blot (отбелязани в доклада на EMA и в статията на Patel) е, че „те [BioNTech] значително са увеличили усилването и повечето хора правят това, за да скрият „мръсните ленти“. Там вероятно има 5 ленти [в една дебела лента, която изглежда уникално]“. Позовавам се на това информативно интервю по-нататък в настоящия доклад.
Това поражда въпроса: дали BioNTech/Pfizer са извършили умишлено прикриване на своите резултати от „Western blot“, като са представили на регулаторните органи манипулирани версии (на автоматични Western)? Може би става дума за изкопиране за FDA и за манипулиране на нивата на насищане за EMA? И още по-важно: как регулаторите са приели тези „Western blots“ като основно доказателство, за да демонстрират верността и последователността на продукта на BioNTech и Pfizer?
Свързахме се с ЕМА, за да получим отговор на опасенията, изразени в това разследване. Техният служител по пресата отговори със следното изявление: „Тези цифри [изображения на Western blot] бяха извлечени от представеното досие и вмъкнати в доклада за оценка, което доведе до загуба на качеството на изображението. Освен това софтуерът за редактиране, използван от ЕМА за подготовка на документи за публикуване след искане за ATD, оказва влияние върху резолюцията на документите.„
По отношение на валидирането на методите, аналитичните методи Western Blot, използвани в проучванията за характеризиране, са били предварително оценени по време на първоначалното условно заявление за разрешение за пускане на пазара като част от „оценката на историята на развитие и сравнимостта“ и са били счетени за подходящи за тази цел.
FDA, Pfizer и BioNTech не отговориха за коментар.
Параметри за качество, установени месеци след издаването на разрешението за пускане на пазара
Причината титулярят на разрешението за пускане на пазара (BioNTech) да проведе допълнителна серия от тестове е, че условното разрешение за пускане на пазара е било издадено въз основа на изпълнението от титуляря на разрешението за пускане на пазара на специфични задължения (като например допълнителни данни за по-нататъшно характеризиране на съкратените и модифицирани видове мРНК), наложени от ЕМА. Към момента на издаване на разрешението за употреба няколко въпроса, свързани с CMC (химия, производство и контрол), бяха изтъкнати като основни проблеми от EMA, по-специално намаляването на целостта на мРНК (наличие на съкратена/фрагментирана мРНК – без критичен атрибут, 5′ край и/или поли(А) опашка) на търговските партиди в сравнение с тези, използвани в клиничните изпитвания. „Решението“ на този основен проблем беше да се намалят критериите за приемане на фрагментирани/съкратени образци мРНК до 50 %, което регулаторните органи просто отхвърлиха.
Канадският фармацевт Мария Гучи, доктор по фармация, която има над 30-годишен опит в болници, общини и правителства, направи независим преглед на проблемите с качеството на ваксините на Pfizer/BioNTech, установени от Европейската агенция по лекарствата, в информативна видеопрезентация. В разговора си с Гутчи тя повдигна други важни въпроси: „Едва през май 2021 г. [5 месеца след издаването на разрешението] OCABR установи параметрите за качество и, което е по-важно, стандартизацията на използваните тестове. Един от проблемите, които установихме, беше, че при пускането на пазара много от тестовете, използвани за определяне на качеството и идентичността, бяха „вътрешни“ тестове на BioNTech. Регулаторният орган не може да приеме това. Те трябва да бъдат валидирани, така че да са последователни, възпроизводими и надеждни.“
OCABR е съкращение от Official Control Authority for Batch Release (Официален контролен орган за освобождаване на партиди), който определя насоките за разрешените ваксини за хора в ЕС. Обърнете внимание на датата май 2021 г., отбелязана в документа на OCABR, показан по-долу.

Фактът, че OCABR е определил първите параметри за качество на ваксина за хуманна употреба зашеметяващите 5 месеца след издаването на CMA, е безпрецедентен. Второ, фактът, че тези тестове (анализи) е трябвало да бъдат валидирани, е забележителен.
Съмнителни „вътрешни“ тестове
Струва си да се отбележи, че загрижеността на Гучи относно „вътрешните“ тестове на BioNTech е споделена и от проверяващия от ЕМА в изтеклия доклад за продължаващия преглед на докладчика от ноември 2020 г. малко преди предоставянето на CMA.

Текст изображение: Коментари на оценителя по S.4.2 и S.4.3 Аналитични процедури:
S.4.2:
Общият коментар, който се отнася за няколко/всички описания на аналитичните методи в този раздел, е, че са дадени доста кратки подробности. Някои от анализите не са представени достатъчно подробно и често описанията на методите се основават на „примери“ за процедури, контроли и стандарти, както и на „типични“ работни параметри на системата (OC). Това пречи на пълното разбиране на действието, а понякога и на научната основа на анализа. Освен това, тъй като някои от тези анализи не са стандартни и сложни, това пречи на оценката на пригодността. Липсата на достатъчно информация за критични реактиви, стандарти или оборудване възпрепятства регулаторния контрол на критичните аспекти на анализите. Повдигнати са няколко опасения по отношение на конкретни анализи, като се изисква да се подчертаят критичните процедури, реактиви, стандарти и оборудване (вж. по-долу).
*За всички вътрешни аналитични процедури, използвани при издаването на DS, описанията на методите се основават на „примери“ за процедури, контроли и стандарти, както и на „типични“ параметри на работа на системата. Тези термини пораждат несигурност по отношение на етапа на разработване и контрола на критичните етапи на тези анализи. Очаква се аналитичните методи, използвани при контрола на DS, да бъдат финализирани. От заявителя се изисква да потвърди това и да актуализира съответните части на досието с недвусмислени описания на методите и допълнителни подробности, ако е необходимо. Заявителят следва също така да потвърди, че всички съществени промени в аналитичните процедури ще бъдат заявени в процедура за промяна. Досието следва да бъде съответно актуализирано.
Позовавайки се на ръководния документ на FDA от 2016 г. относно „Интегритета на данните и спазването на CGMP„, той гласи: „През последните години FDA все по-често наблюдава нарушения на CGMP, свързани с целостта на данните по време на инспекциите на CGMP. Това е обезпокоително, тъй като осигуряването на целостта на данните е важен компонент от отговорността на индустрията да гарантира безопасността, ефикасността и качеството на лекарствата и способността на FDA да защитава общественото здраве.“
Изглежда, че разглеждането на нарушенията на целостта на данните от страна на FDA като „обезпокоителни“ изчезва – чрез лесното приемане на данните на BioNTech, които изглеждат като „изкопирани“. Може би за тях това е било просто упражнение за попълване на квадратчета, за да изглежда, че полагат дължимата грижа за „защита на общественото здраве“.
„Неочаквани“ ленти, които се появяват в истинските Western blots на BioNTech
Сред всички компютърно генерирани „Western blots“ BioNTech всъщност представи два автентични Western (вторият ще бъде разгледан по-късно), което доказва, че знае как да ги прави. В изтеклия доклад за оценка „Rolling Review“ на репортера на EMA са отправени следните критики към изследването 20-0211 на BioNTech„по отношение на резултатите от Western blot“, отбелязани по-долу.

Текст изображение:
„В изследване 20-0211, по отношение на резултатите, получени от Western Blot, трябва да се предостави полуколичествен анализ на резултатите, за да се подобри четливостта на протеиновата експресия, а в анализа на Blot заявителят трябва да добави някои липсващи научни сведения и обяснения (CoRapp 8):
а.Наличието на две ивици за BNT162b2 ARN (съответно 100 KDa и 190 KDa)
б. 76,5 kDa не се наблюдават нито в контролните ленти на BNT162b2, нито в S1, а пълният S протеин при 141,14 kDa също не се наблюдава в лентата на BNT162b2.
в. Липсата на важна експресия за S1 протеин ctrl при 76,5 Kda“
През февруари миналата година изследване 20-0211 (изследването, посочено по-горе), проведено от BioNTech, е публикувано като част от разпореденото от съда изхвърляне на данни от Pfizer. Силно разкриващото автентично Western Blot, показано в това изследване, може да се види по-долу.

От доклада за оценка на EMA от ноември 2020 г. знаем, че агенцията е отбелязала неочакваните молекулни тегла (измерени в kDa) на двете протеинови ленти, показани в Western Blot, съответно 190kDa и 100kDa, което я е накарало да поиска обяснение от BioNTech. Сега, пълният протеинов шип има молекулно тегло 141 kDa, а S1 (белтъчна субединица на шипа) има молекулно тегло 76,5 kDa, което е използвано като контрола. Обърнете внимание на горната фигура, че в лентата на BNT 162B2 няма белтъчни ивици с нито едно от тези очаквани молекулни тегла и че очакваното молекулно тегло 76,5 kDa на протеина S1 не е наблюдавано в контролната лента S1. Тези аномалии изпъкват пред регулатора, но по някакъв начин разработчикът на ваксината, BioNTech, който със сигурност би трябвало да знае очакваното молекулно тегло на протеина на пълния шип, тъй като неговият мРНК продукт е трябвало да го кодира, дори не ги разпознава.
За да задълбочи пълния си провал в решаването на тези проблеми, BioNTech написа изключително неточно описание на своя Western Blot – всъщност точно обратното на това, което беше показано на снимката: „BNT162b2b2 има очакван размер от 141,14 kDa“ и „белтъкът на субединицата S1 на SARS-CoV-2 (76,5 kDa) е използван като положителна контрола„.
Това предполага, че е вероятно протеиновият шип S1S2 да не е бил експресиран от модифицираната с ваксина мРНК или ако е бил, може би са били експресирани и други аберантни протеини, които произхождат от фрагментирани/отрязани молекули РНК в лекарственото вещество.
Липса на секвениране на генома и проблеми с метилпсевдоурина N1
Когато е попитан за проблемите с качеството на ваксината на Pfizer-BioNTech, изследователят в областта на геномиката Кевин МакКернан дава следния отговор:
„Не разполагаме с ДНК секвенция на тези партиди. Това е абсолютна лудост! Изхождайки от проекта за човешкия геном, ние публикуваме по една секвенция на всеки 24 часа, за да сме сигурни, че светът има достъп до най-новите данни, идващи от проекта за човешкия геном. Като превъртите до днешния ден не можете да намерите никакво секвениране на партидите от генома„.
Удивително е, че регулаторните органи са разчитали на тези манипулирано изглеждащи Western blot тестове от BioNTech, вместо да изискват секвениране на генома на партидите, за да докажат тяхната последователност и вярност.
МакКернън продължи да разглежда проблемите, причинени от променената РНК, синтезирана с помощта на променена база:„Имаме продукт на мРНК, в който всеки уридин е заменен с N1 метилпсевдоурин, който организмът никога не е виждал преди. Те [BioNTech и Pfizer] избраха стоп кодони, които са най-известните за създаване на грешки. Те [са били наясно с проблема, но не са го отстранили правилно. Това означава, че когато рибозомите отиват да прочетат шаблона, са много объркани, защото никога преди не са го виждали.“
МакКернън е съавтор на статия с д-р Питър Маккълоу и Антъни Кириакопулос, озаглавена „Differences in Vaccine and SARS-CoV-2 Replication Derived mRNA (Разлики в мРНК, получена от ваксината и репликацията на SARS-CoV-2): Авторите стигат до заключението, че „промените в синонимните кодони, вградени в мРНК на ваксините, могат да променят очакваната конформация на кодирания протеин, тъй като скоростта и ефективността на транслацията могат да доведат до различна протеинова гънка… Стратегиите за оптимизиране на кодоните за разработване на мРНК ваксини могат да доведат до имунна дисрегулация, да повлияят на епи-транскриптомната регулация и да доведат до прогресия на заболяването„.
Модифицираният уридин (N1 метилпсевдорин) е включен в мРНК, за да се заобиколи вроденият имунен отговор и да се насърчи транслацията на протеина. Въпреки това, в доклада на ЕМА от ноември 2020 г. за текущ преглед (страница 61) е повдигнат въпрос за потенциален риск за безопасността при модифицираната РНК (modRNA), вж. по-долу.
„MODRNA съдържа 1-метил-псевдоуридинова замяна с уридин. Това заместване намалява разпознаването на РНК на ваксината от сензорите на вродената имунна система. Въпреки това не беше представено допълнително обсъждане на риска от автоимунни реакции, предизвикани от модРНК. Заявителят се приканва да обсъди по-подробно възможността мРНК ваксината да предизвика потенциални автоимунни реакции и как възнамерява да оцени възможната поява на такива реакции.
Не е известно дали BioNTech някога е оценявал потенциалния риск за безопасността от автоимунни реакции, предизвикани от модифицирана уридина или транслирани протеини (различни от протеиновия шип), тъй като към август 2021 г., с изтекъл краен срок през юли 2021 г., това все още не е направено. (Вж. снимката по-долу, страница 13 от доклада на CHMP на EMA от август 2021 г.)

Текст изображение:
„трябва да се предостави информация за преобладаващите видове. Трябва да се оцени всяка хомология между преведените протеини (различни от протеина на шипа) и човешките протеини, които поради молекулярна мимикрия могат да предизвикат автоимунен процес. Срок за изпълнение: юли 2021 г. Междинни доклади: Март 2021 г. и на месечна база.“
Обезпокоителни са констатациите на най-голямото по рода си проучване от Университетската болница „Крал Фахад“ в Хобар, Саудитска Арабия, свързващо мРНК ваксините с отключването на автоимунни заболявания, които TrialSite наскоро съобщи. „Молекулярната мимикрия“, посочена като проблем в доклада на ЕМА по-горе, е същата хипотеза, изказана в проучването като механизъм, свързан с това, че мРНК ваксините предизвикват автоимунен процес.
Потенциални проблеми, произтичащи от производствения процес
Фигурата по-долу показва опростения изглед, използван за популяризиране на начина на действие на мРНК ваксините.
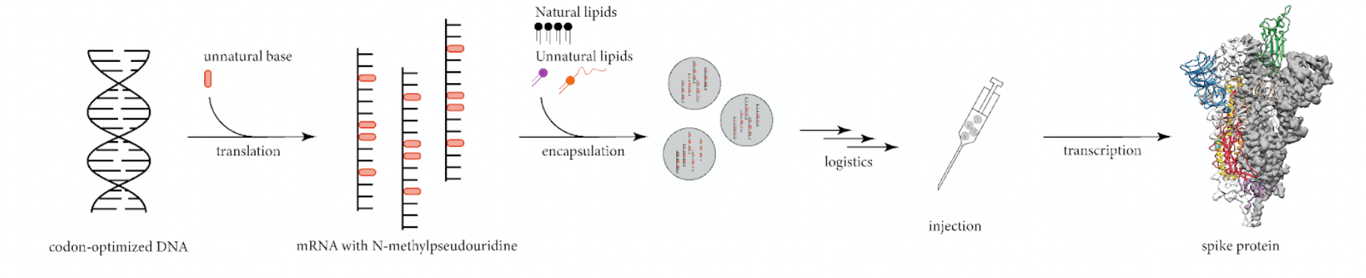
В действителност процесът е силно променлив, което от своя страна води до създаването на силно променливи протеинови продукти, вж. фигурата по-долу.

Всяка стъпка от производствения процес може да внесе неизвестни примеси и неизвестни грешки, от „невярната“ транслация на оптимизираната за кодони ДНК, която може да генерира (неинтактни) фрагменти на мРНК, до „невярната“ транскрипция на сместа от мРНК в човешкото тяло, която може да генерира неочаквани протеинови продукти.
МакКернън продължи да обяснява по-подробно процента на грешките и техните последици: „Моята оценка е, че има по една грешка на молекула ваксина – като се има предвид, че във всяка инжекция има 14 трилиона молекули – не знаем какво означава това от имунологична гледна точка. Ето защо трябва да има секвениране на партида по партида, преди да се инжектира продукт, за който се знае, че произвежда нови протеини в човека„.
Модифицираната мРНК с пълна дължина на ваксината на Pfizer-BioNTech, кодираща протеиновия шип, е дълга ∼4300 нуклеотида, nt. Всичко, което е по-малко, се счита за фрагментиран вид мРНК, който EMA класифицира като „свързан с продукта примес“. Това води до друг скандал, известен като „Humpgate“.
Скандалът Humpgate
Скандалът „Humpgate“ може да се разглежда като предшественик на „Blotgate“. Докато Blotgate се фокусира главно върху фалшиво изразените протеинови ленти на ваксиналната мРНК, наблюдавани в BioNTech Westerns, Humpgate се отнася до съкратените видове мРНК, докладвани от ЕМА и други регулаторни органи. Името идва от „гърбиците“ (humps), които се виждат на изображението в публикацията в социалната мрежа по-долу.
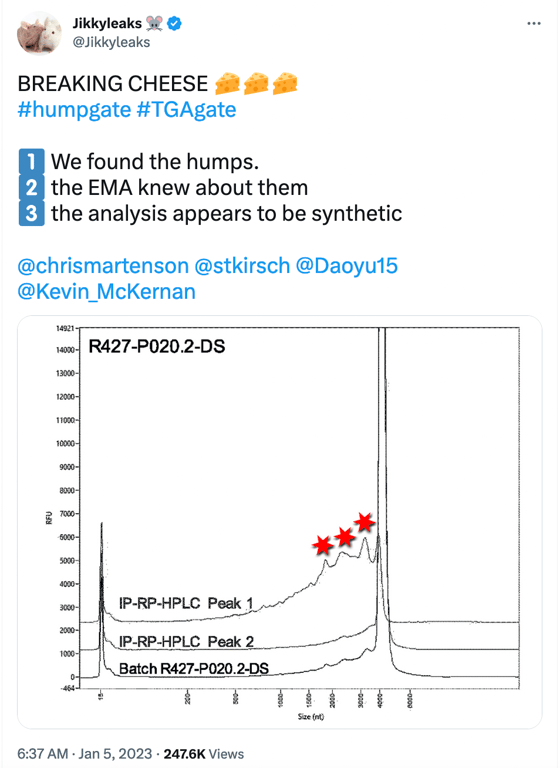
Трите „гърбици“, обозначени с червени звезди, представляват съкратени/фрагментирани видове РНК със съкратена дължина (nt) <4000nt. Изображението по-горе е електроферограма на фрагментния анализатор (който е горното изображение на Фигура 2, показана по-долу), взета от страница 15 на доклада на ЕМА, написан през лятото на 2021 г., който BioNTech предприе, за да изпълни SO1 (специфично задължение 1), поставено от ЕМА, която поиска допълнителни данни за по-добро характеризиране на съкратените и модифицирани видове мРНК.

От Опит 1(R427-P020.2-DS, партида за клинично изпитване, горната снимка) и Опит 2 (20Y513C501, партида за PPQ, долната снимка) са взети фракционирани проби, като е използвана RP-HPLC с йонно сдвояване, за да се характеризират допълнително интактните (с пълна дължина) и фрагментираните видове мРНК. И при двете партиди (Опит 1 и 2) се наблюдават малки неравности, водещи до голям пик с размер приблизително 4300 nt, който представлява вида на мРНК с пълна дължина. Графичната линия, обозначена като Пик 1, показва „пречистения“ повторно анализиран материал, съставен само от фрагментарни видове мРНК (това са малките неравности, наблюдавани от лявата страна на големия пик с размер приблизително 4300 nt в пробата от партидата), а Пик 2 е „пречистеният“ повторно анализиран материал, съставен от непокътнати видове мРНК, наблюдавани при „големия пик“.
Същата електроферограма може да бъде намерена в статията, публикувана през януари 2023 г., Patel et al. (вж. изображението по-долу, публикувано 18 месеца след доклада на ЕМА). Авторите Patel et al., обаче, цитират изследването си като актуално, докато то представлява преработена версия на отговора на самата компания Pfizer/BioNTech на въпросите на FDA и EMA отпреди 18 месеца. Фактът, че авторите представят изследването си като „независимо“ и „актуално“, когато технологията ProteinSimple Wes, използвана в тяхното изследване, е преустановена от 30 юли 2021 г., е най-малкото неискрен.
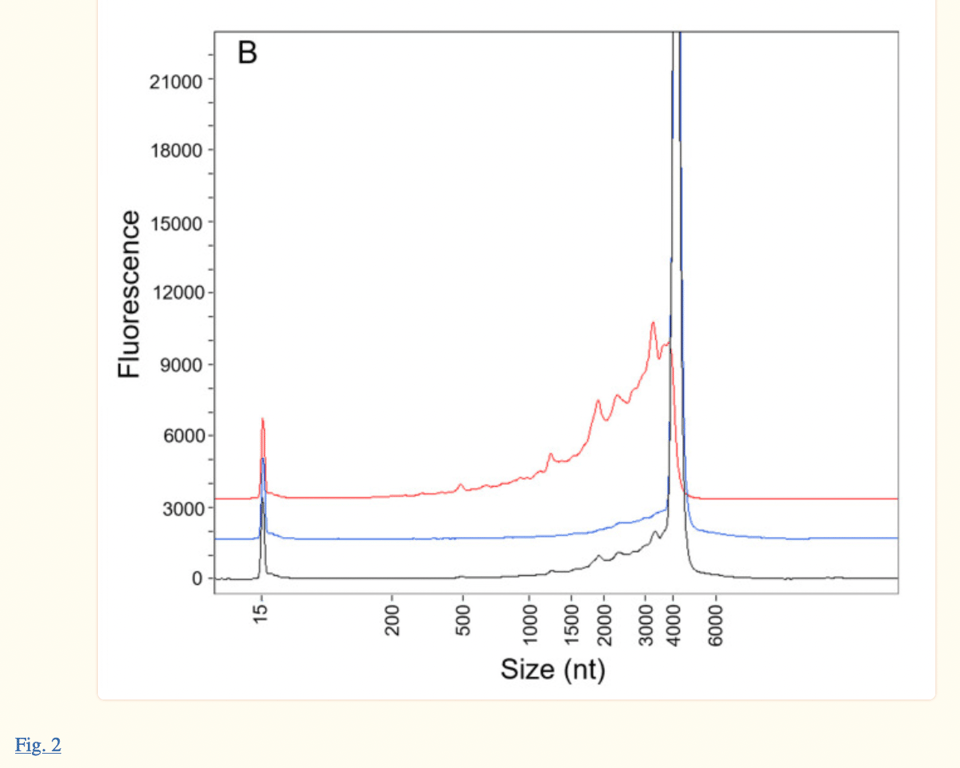
Както в статията на Patel et al, така и в статията на EMA се повдига въпросът за гърбиците, наблюдавани от лявата страна на основния пик при около 4300 nt. В доклада на ЕМА се посочва, че „(Фигура 2) показва, че връх 1 се състои почти изцяло от фрагментирани видове, което съответства на данните, предоставени по-рано в оценката на отговора на CHMP Q01-Quality 11-Dec-2020“.
Проблемът с хипотезата на BioNTech
Начинът, по който BioNTech увери EMA, че тези съкратени видове РНК няма да могат да поддържат транслацията на протеини, така че съкратените видове, които се виждат като „гърбици“ в електроферограмите, да не се считат за проблем, беше чрез извършване на нови Western Blot тестове, за да докаже, че РНК „транскриптите изискват както 5′-кап, така и поли(А), за да поддържат транслацията на протеини…“

Ето как изглежда РНК с пълна дължина BNT162b2. В началото на транскрипта на РНК е добавен 5′-кап, а в края на транскрипта е добавена 3′-поли(А) опашка. Рибозомите четат транскрипта от 5′ към 3′ посока.

Фигурите по-долу (6 и 5) са взети от доклада на EMA CHMP от август 2021 г.

Празните линии, показани в панелите на лекарствените вещества, които не са Poly(A), са достатъчни, за да докажат на регулаторния орган, че РНК, в която липсва Poly(A), няма да може да експресира протеиновия шип S1S2. Проблемът с този анализ обаче е, че той не потвърждава, че други аберантни протеини (което беше първоначалната загриженост на ЕМА) могат да бъдат експресирани от тази съкратена РНК, тъй като са използвани само специфични за S1 и S2 домейна антитела за откриване. Western blot-ът, показан по-долу, има същия проблем. Този анализ е използван, за да се увери регулаторният орган, че транскриптът на РНК, при който липсва 5’cap, не може да експресира протеиновия шип S1S2.
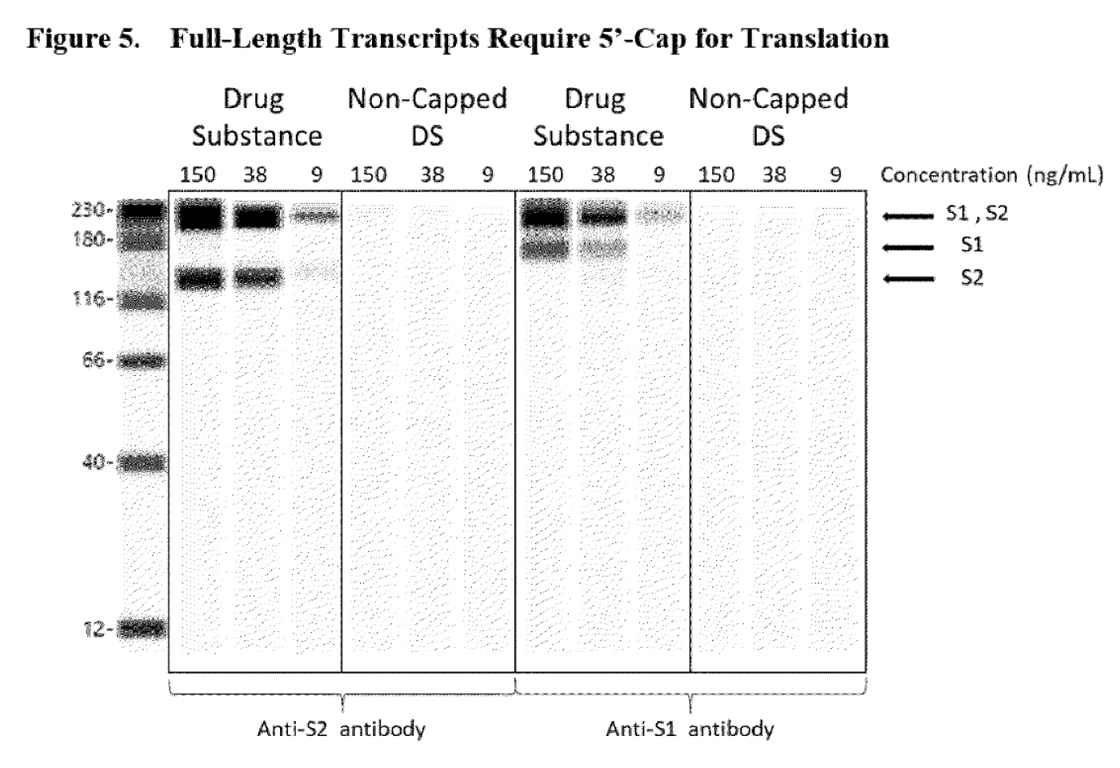
Освен това се предполагаше, че фрагментираният вид РНК е резултат от преждевременно спиране на транскрипцията или хидролизата на мРНК (когато молекулата се разпада на две части при реакция с вода), вж. откъса по-долу.
„Свързаната с това оценка на безопасността показа, че вероятността фрагментираните видове да са получени в резултат на преждевременно спиране на транскрипцията или хидролизата на мРНК. Като такива, фрагментираните видове предимно нямат както 5′-кап, така и поли(А) опашките, необходими за експресията на протеини.“
Източник: Доклад на EMA CHMP от август 2021 г
Това създава фалшиво чувство за сигурност, че съкратеният транскрипт на мРНК може да има само 5’кап или поли(А) опашка, но никога и двете.
Миражът на теста за разграждане
Потенциалът на съкратените РНК транскрипти да произвеждат протеини беше допълнително изследван от BioNTech по искане на регулаторния орган. Интересното е, че партидата (1071509) е била умишлено подбрана и умишлено разградена чрез излагане на високи температури, за да се получат проби с фрагментирани видове. Показаният по-долу Western blot е вторият традиционен, представен от BioNTech. То показва, че способността на транскрипта на РНК (когато е разграден от топлина, следователно фрагментиран) да експресира протеин става по-ниска.
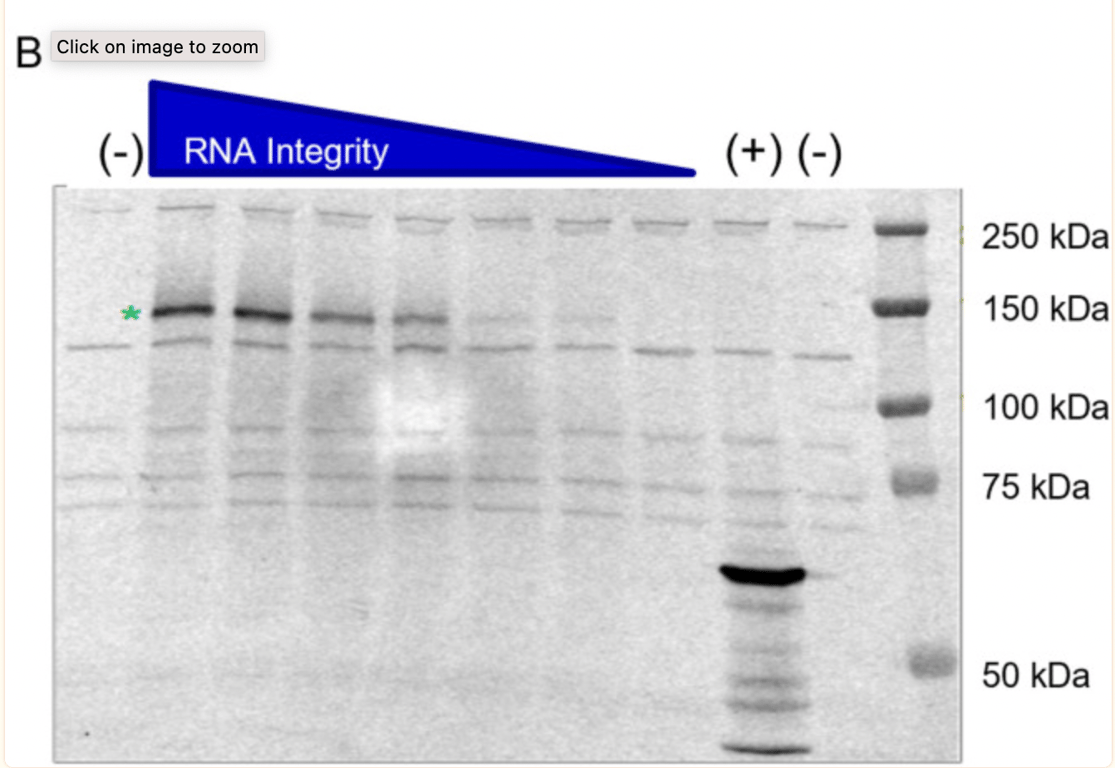
Зелената звезда показва, че пробата BNT162b2, която не е разградена от топлина (без топлина, непокътната/висока цялост на РНК), произвежда белтък от около 140 kDa, което съответства на очаквания размер на агликозилирания белтък S1S2. BioNTech заявява, че „Не са открити съкратени или други протеинови видове извън фоновите ленти, наблюдавани в отрицателната контролна проба“ , но в лентата на неразградената проба се виждат протеинови ленти и не се дава обяснение какви са те.
В интервюто на МакКернън той обяснява: „Това, което са направили в изследването си, е, че са взели мРНК и не са я фрагментирали, както се получава при производствения процес, а са я нагрели! Причината, поради която са фрагментирани, е, че полимеразите засядат на тези ненативни (модифицирани) бази при синтеза на РНК, така че се получават тези по-къси части от РНК в производствения процес, а този процес вероятно варира в зависимост от нуклеотидите, които получават от доставчиците си“.
В доклада на ЕМА от август 2021 г. е направено ново изискване, което BioNTech трябва да изпълни – искане за извършване на същото охарактеризиране за поне три допълнителни партиди тозинамеран (модифицирана мРНК, лекарствено вещество). Както можете да видите, това изискване не е било изпълнено до август 2021 г.

А според последната актуализация (2 февруари 2023 г.) Комисионата: EPAR доклад, това задължение все още остава неизпълнено.

Текст изображение:
„По отношение на SO1 титулярят на разрешението за търговия е предоставил допълнителни данни за характеризиране, както е поискано.
a/ Потенциалът на съкратените транскрипти да произвеждат протеини/пептиди беше допълнително изследван, като беше използвана безклетъчна ин витро експресионна система. Не бяха открити съкратени или други протеинови видове извън фоновите ленти, наблюдавани в отрицателната контролна проба. Титулярът на разрешението за търговия ще допълни упражнението за характеризиране, използвайки безклетъчна инвитро система за транслация, с допълнителни партиди тозинамеран.“
МакКернън се позовава и на работата на Патерсън и др. която открива мутантни версии на протеиновия шип при ваксинирани хора, които не съществуват при неваксинирани хора, които са имали COVID-19 и това е тревожно. Това може да се приеме като данни от наблюдения в реалния свят, които показват, че мутантните (аберантни) версии на протеиновия шип се транслират от модифицирана с ваксина мРНК.
В заключителния си коментар МакКернън казва: „Хората от регулаторните органи са заспали на волана. Те са напуснали кормилото и са го оставили да се движи на круиз контрол“.
Не мога да не се съглася.
Първоначално публикувано в Trial Site News
Suggest a correction






